Ionen, ionische Bindung Unterschied?
Moin,
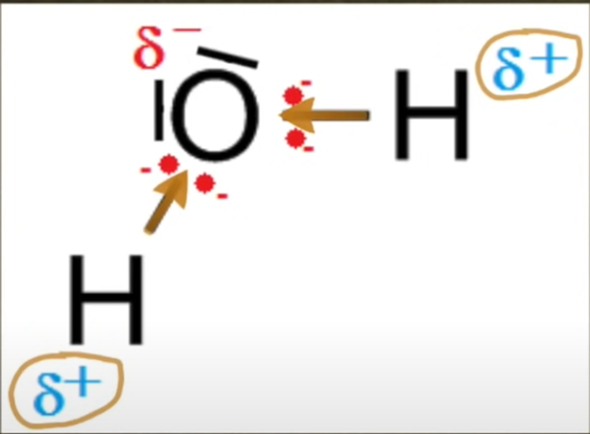
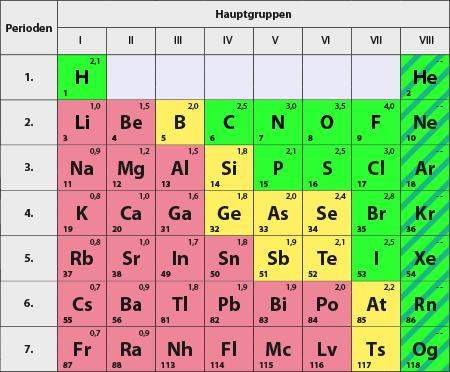
bei Molekülen unterscheidet man ja zwischen polaren und unpolaren. Bei Elektronegativitätdifferent zwischen 0 und 0,6 oder sowas, ist es umpolar, von 0,6 bis 1,7 polar und ab 1,7 sind es ja ionische Bindungen. Aber was sind ionische Bindungen? Ist es dann immer noch ein Molekül oder sind genau das Ionen, also Kationen und Anionen?