Woran erkennt man ob eine As basisch , Sauer , polar oder unpolar ist?
Gibt es da irgendwelche Tricks mit denen man das schnell und richtig herausfinden kann ??
4 Antworten
Der Teil der auch im Glycin drin is is bai allen alpha-AS, also allen proteinogenen gleich, den kannst du ignorieren. Du schaust dir also nur den Rest an.
Sauer isses wenn im Rest eine Carbonsäure (-COOH) hängt, die kann ein H+ abspalten -> sauer.
Basisch wenn du auf den rest irgendwie ein H+ draufprügeln kannst (z.b. Amin auf ein quarternäres Ammonium)
Wenn der Rest nur Cs und Hs hat oder die Teilladungen sonst nicht wirklich aufgeteilt sind (Methionin z.b.) -> unpolar
Wenn die ladungen relativ stark aufgeteilt sind aber du weder leicht ein Proton rein- noch rausprügeln kannst isses polar und neutral. Da zählt auch Glycin (Rest= H) dazu dass muss man sich halt merken.
Sollte am Ende dann irgendwas in der Art rauskommen:
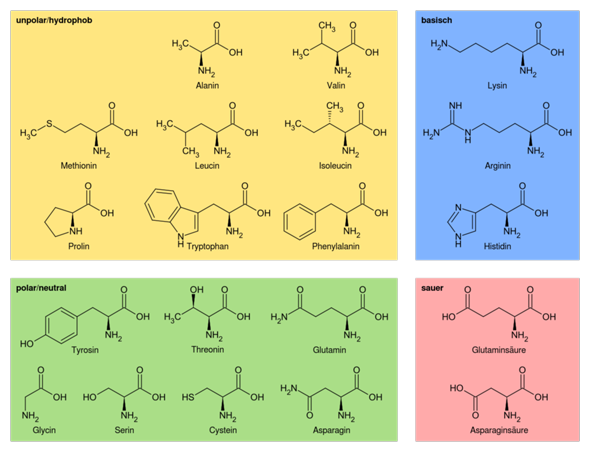
Soweit alles klar?
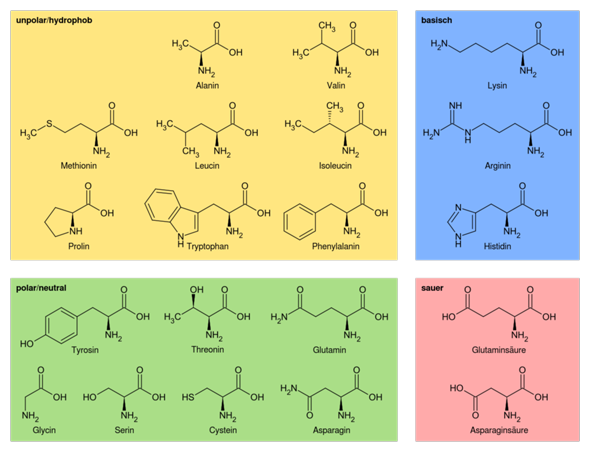
Konzepte polar/unpolar und sauer/basisch generell bei organischen Molekülen ist klar? Also du verstehst zum Beispiel warum Essigsäure sauer und Ethylamin basisch ist? Aceton ziemlich polar und z.B. Hexan unpolar? Weil wenn nicht würd ich mir zuerst das anschauen.
Naja ich verstehe das alles nicht wie man das bestimmen soll/ kann
Würde mir dann halt die grundkonzepte nochmal geben.
Gibt da gute Videos zu, oder halt ein Lehrbuch Organik für Nebenfach und Lehramt besorgen, die sind halbwegs verständlich und gehen da gut drauf ein.
Die Kürzestfassung, die halt nicht annähernd zum verstehen reicht:
Backbone ignorieren, nur der Rest (also das was ich oben im ersten Bild rot markiert habe ) wird betrachtet
Carbonsäuren immer sauer.
Freie Aminogruppen und Imidazol basisch.
Alkane, Aromaten, Thioether neutral unpolar
Amid, Alkohol, Thiol und (arguably) Phenol sind polar neutral.
Der Trick ist lernen! Englisch lernt man auch nicht durch Tricks. Da muss man Vokabeln und Grammatik lernen. Das ist in anderen Fächern nicht anders. In Chemie muss man halt die üblichen Formeln und die Eigenschaften von Verbindungen lernen. Anders geht das nicht.
Der Trick ist, die funktionellen Gruppen zu kennen. Jede funktionelle Gruppe hat bestimmte Eigenschaften, so ist die OH-Gruppe polar, wie in Alkoholen.
Lies dir die Super-Antwort vom unversalprofi doch mal durch und versuche zu verstehen: extra COOH -> sauer, extra NH2/N mit freiem e-Paar -> basisch
Ich verstehe es leider irgendwie imemr noch nicht so ganz :(