Dipol Verbindungen?
Die Fragestellung lautet zu kennzeichnen ob es sich bei folgenden Verbindungen um Dipolverbindungen handelt oder nicht:
OF2
CF4
H2O
HCl
CH2Cl2(Dichlormethan)
CHCl3(Chloroform)
Helft mir bitte auf die Sprünge woran ich das genau erkenne. Soweit ich weiß ist es eine Dipol Verbindung ab einer bestimmten elektronegativitätsdifferenz(jedoch wüsste ich nicht ab welcher weil verschiedene Quellen verschiedenen Antworten liefern). Das würde aber wieder die Frage aufwerfen was der Unterschied zwischen den letzten beiden Verbindungen ist, da beide die selben Komponenten haben, obwohl es mehr Chlor Atome gibt, was bedeuten würde, dass über alle Atome summiert eine höhere Elektronegativitätsdifferenz herrscht, da die Verbindungen jeweils mit dem Kohlenstoffatom entstehen. Ich freu mich auf eure Antworten.
1 Antwort
Hi,
zunächst ist es hilfreich, sich die Strukturformeln der entsprechenden Moleküle aufzuzeichnen (oder im Zweifel zu ergooglen, wenn man sich nicht sicher ist).
Ein Dipol liegt dann vor, wenn du polare Bindungen hast und durch das Molekül eine Art "Achse" hindurchlegen kannst, die das Molekül in eine positiv polarisierte und eine negativ polarisierte Seite teilt. Es hängt also von den Elektronenaktivitäten und der Molekülgeometrie ab.
Beispielsweise hast du bei Wasser eine gewinkelte Struktur mit zwei posidiv polarisierten Wasserstoffatomen und einem negativ polarisierten Sauerstoffatom. Durch das Molekül kannst du eine Achse legen; Sauerstoff bildet die negative Seite, Wasserstoff die positive. Also ist Wasser ein Dipol.
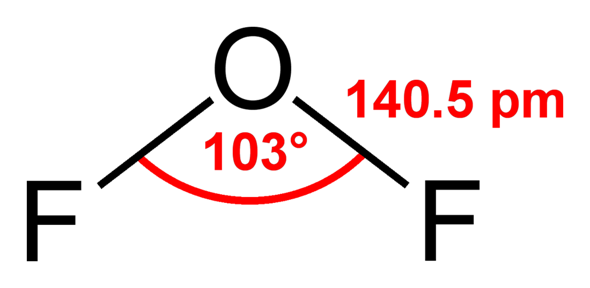
OF2 sieht so aus:
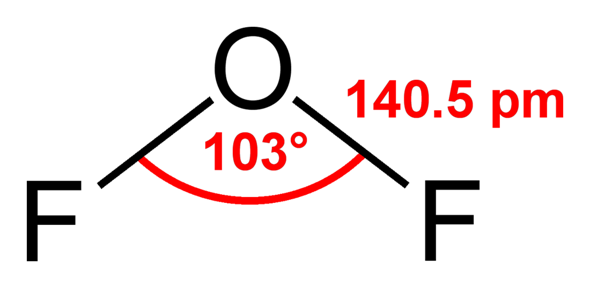
Fluor hat eine Elektronegarivität von EN(F) = 4,0 und Sauerstoff EN(O) = 3,5. Diese Bindung ist also schwach polar. Horizontal kannst du durch das Molekül eine Achse legen. Sauerstoff ist positiv polarisierte, Fluor negativ – also liegt ein Dipol vor.
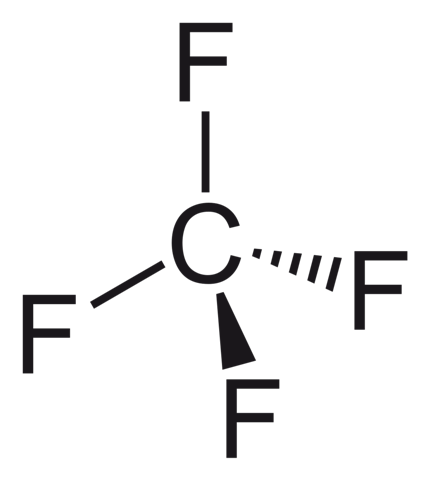
CF4 hat die folgende Molekülstruktur:
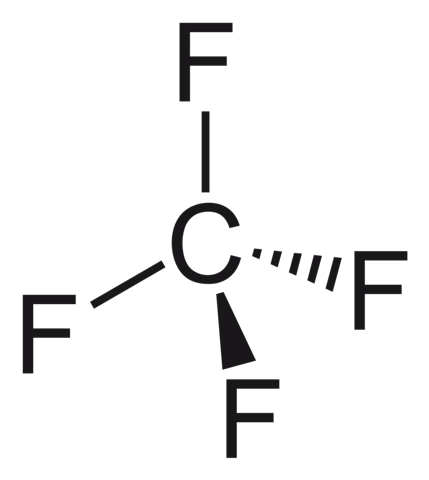
Die Bindungen von CF4 sind zwar allesamt stark polar, da die Elektronegativität von Kohlenstoff nur 2,5 beträgt, allerdings ist CF4 tetraedrisch aufgebaut. Das heißt, du kannst das Kohlenstoffatom nicht als Pol separieren, da es genau mittig im Molekül ist und von allen Seiten durch Fluoratome umschlossen ist. Somit liegt bei CF4 kein Dipol vor.
Den Rest schafft du sicher selbst! :)
LG