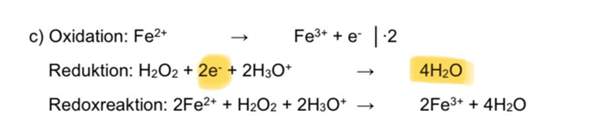
Hey zusammen, ich bereite mich gerade für mein Chemie LK Abitur vor. Bei der Vorbereitung habe ich nun aber ein kleines Problem entdeckt. Als wir das Thema Redoxreaktionen im Unterricht hatten, haben wir folgende Reaktion aufgeschrieben: OX: MnO2 + 6H2O --> MnO4- + 3e- + 4H3O+. Bei dieser bin ich mir beim Elektronenausgleich nicht sicher. Mn (Edukt) hat ja Oxzahl 4 und Mn (Produkt) 7. Dementsprechend klar 3 Elektronen zum Ausgleich, aber nimmt man nicht noch die negative Ladung vom MnO4 mit in diese Rechnung rein? Demnach bräuchte man nur 2 Elektronen. Ich denke eigentlich nicht, allerdings ergibt sich mir dann daraus aus einer anderen Aufgabe keinen Sinn:
NH4+ + NO2- ---> N2 + 2H2O
Klar, NH4+ wird oxidiert und NO2- reduziert, aber die Teilgleichungen machen bei mir mit Elektronenausgleich, H3O+ Ausgleich und H2O Ausgleich keinen Sinn.
Bei den Teilgleichungen dann am besten auch mit Elektronen und allem antworten, denn diese Sachen wegkürzen ist nicht das Problem, sondern das Verständnis dahinter.
Ich bedanke mich im Voraus schonmal für alle netten Antworten!