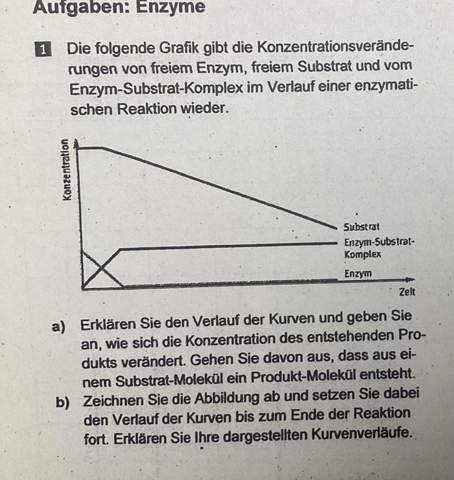
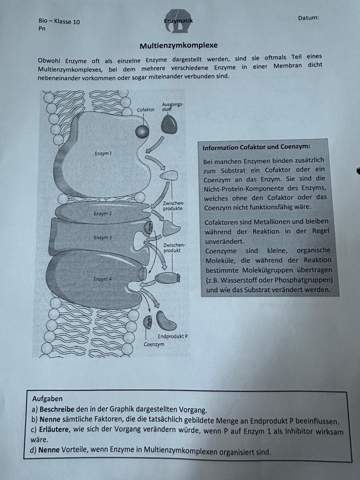
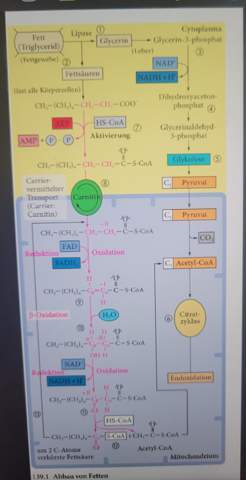
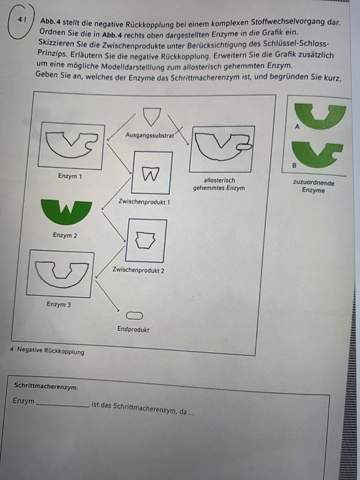
Hey,
schreibe bald eine Bioklausur (zehnte Klasse) und Thema ist (unter anderem) Enzymatik. Verstehe das meiste nur bei diesem k(m)-Wert und darauf basierendem Stoff bin ich mir unsicher. Deshalb ersteinmal allgemein die Frage, ob diese Aussage(n) richtig sind, dann kann ich darauf basierend weiter lernen.
"Den Wert der Substratkonzentration bei halber Reaktionsgeschwindigkeit nennt man K(m)-Wert.
Je kleiner dieser ist, desto schneller finden Enzyme und Substrat zueinander. Ist das der Fall spricht man von einer hohen Affinität. Demnach braucht es nicht viele Substrate, um die Hälfte der vorhandenen Enzyme zu besetzten und somit 0.5 V(max)zu erreichen.
Je größer der K(m)-Wert, desto geringer ist die Affinität zwischen den Enzymen und den Substraten. Es braucht also viele Substrate, um die Hälfte der vorhandenen Enzyme zu besetzten.
Daraus lässt sich schlussfolgern, dass bei einem niedrigen K(m)-Wert Enzyme und Substrate schnell aufeinander treffen und dabei einen Enzym- Substrat-Komplex bilden. Bei einem hohen K(m)-Wert dauert dieser Vorgang länger, weil für die selbe Anzahl an zu besetzenden Enzymen mit mehr Substraten gleich viel Zeit beansprucht wird. Einzelne Substrate brauchen hierbei also mehr Zeit um einen Enzym-Substrat-Komplex zu bilden. Es dauert demnach länger bis die maximale Reaktionsgeschwindigkeit erreicht ist."
Ich hab keine Ahnung, ob das so richtig ist, besonders beim letzten Teil bin ich mir unsicher... Kann jemand das eventuell noch einmal erklären (falls das nicht stimmen sollte?)