Frage zu H2O und Verhalten zu porösen Stoffen?
Hallo.
H2O hat ja an sich eine sehr geringe Größe und könnte ja locker durch eine Pore durchdringen.
H2O: Größe => 0,27nm laut ChatGPT
Pore von PTFE z.B.: 1mycrometer
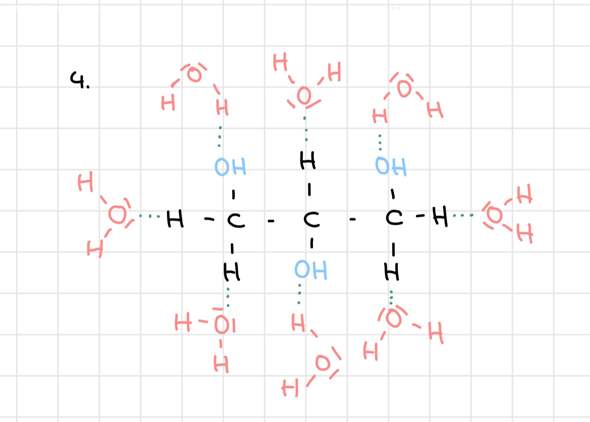
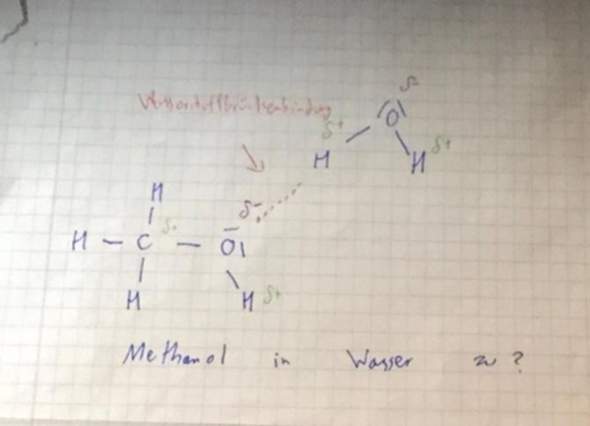
Und das PTFE lässt ja das Wasser dennoch nicht durch. Wasser bildet ja unter Molekülen Wasserstoffbrückenbindungen, welche ja schwach/stark Polar sind? (Das ist ja keine Molekülkette, weshalb ich davon ausgehe, dass es schwach Polar ist. Wegen diese Dipol-Dipol-Anziehungskräfte?)
Und das heißt ja, dass diese Wasserstoffbrückenbindungen gewaltig Groß sind und die Poren ja dann so gar nicht durchdringen können.
Dazu ist ja Teflon auch noch unpolar und sehr stabil? Bedeutet, dass Teflon sich nicht so leicht zersetzt und hohe Energie braucht, um zu zersetzen. Wasser ist ja stark Polar und Teflon ist unpolar (hat das dann auch noch eine Wechselwirkung?).
Wenn Moleküle Wasserstoffbrückenbindungen eingehen, ist es dann ohne Ausnahme IMMER so, dass die dann Poren nicht durchdringen?
Oder warum genau ist PTFE wasserabweisend?
Kann mir jemand genau erklären, wie ich das verstehen kann?
Weil ich stelle mir das so vor, dass wegen der H-Brückenbindung das alles passiert. Dann muss es ja bei allen Molekülen mit H-Brückenbindungen so sein, dass PTFE das nicht durch die Poren lässt. Ist das korrekt?