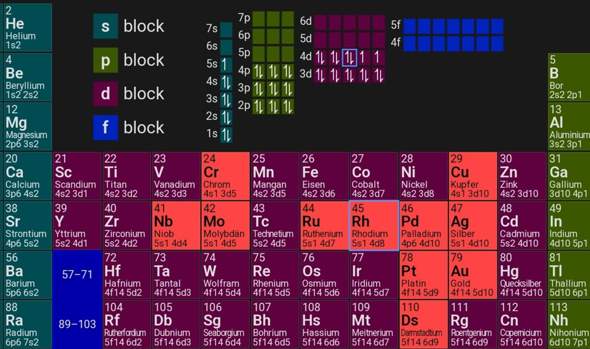
Warum ist Fe^2+ stabil?
Heißt es nicht, dass Übergangsmetalle mit halbvoll oder voll besetztem d-Orbital stabiler sind? So wie die Oktettregel bei den Hauptgruppen?
Werden jetzt von dem Fe die 2 Elektronen aus dem 4s Orbital abgespalten, bleibt schließlich noch 1 Elektron "zu viel" in dem d-Orbital, sodass dass Fe 6 Elektronen im d-Orbital hat.
Aber sollten es nicht möglichst 5 oder 10 sein?