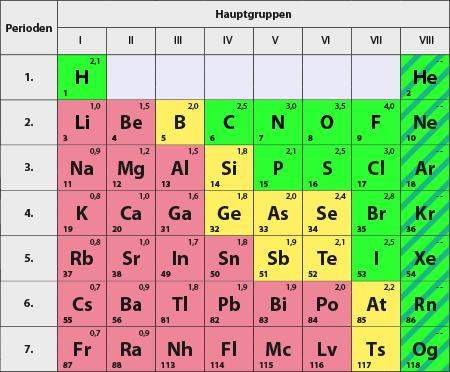
Warum hat Wasserstoff nicht eine höhere Elektronegativität als Fluor?
Während Fluor die größte Elektronegativität mit 4,0 hat, hat Wasserstoff nur 2,2. Und das obwohl beide nur mehr ein Atom brauchen um im Edelgaszustand zu sein. Außerdem ist das Elektron des Wasserstoffatoms in einer kovolenten Bindung näher am Atomkern als bei einem Fluoratom. Erste Vermutung war jetzt, dass Wasserstoff einfach zu wenig positive Ladung durch nur ein einziges Proton besitzt. Aber weshalb hat dann Chlor weniger Elektronegativität als Fluor, obwohl Chlor ja viel mehr Protonen hat?