Wie bestimmt man den pH-Wert von Kaliumacetat in Wasser gelöst?
Hallo,
also genauer gesagt muss man in der Aufgabe den pH-Wert von 12,1g Kaliumacetat in 250ml Wasser gelöst berechnen.
Die Konzentration vom Kaliumacetat (c= 0,492 mol/l) habe ich bereits.
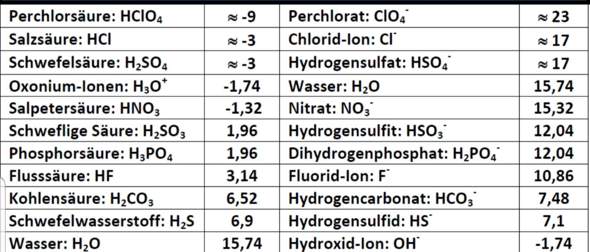
Aber jetzt weiß ich nicht, wie ich den pks-Wert von Kaliumacetat berechne, mit dem ich dann sehe, ob es eine schwache oder starke Säure ist, und dann die entsprechende Formel verwende. Ich bin mir auch nicht sicher, ob es eine Säure ist... mein Gedanke war, dass Kaliumacetat Protonen abgeben kann.. also ist es eine Säure?
Kann mir bitte jemand mit der Aufgabe helfen?