Chemie verbindung von 2 Stoffen?
Hi. ich check das aber es gibt zwei sachen die ich nicht verstehe. Was ich meine ist das zb: Sauerstoff (O) gibt elektronen an ein anderes sauerstoff, man schreibt das mit so doppelpunkten auf die über neben oder unter dem buchstabe, in dem fall O sind. Hier ein beispiel (ist falsch weil mans hier nicht richtig malen kann)…
: O : + : O : gleich / O \ = / O \
also die geben elektronen ab und die punkte der jeweils zwei buchstaben kreist man dann so ineinader ein. hoffe ihr versteht was ich meine. Ist halt molekühl bindung, kovalente bindung usw…
nun meine fragen: woher weiß ich wie viele punkte ich da hin machen muss? Zb. stickstoff hat 3 punkte vor und 2 punkte drüber oder sauerstoff hat 3x doppelpunkte. woher weiß also wie viele punkte ich da machen muss und wo die hin müssen und wie ich die verteilen soll?????
Und die zweite frage ist: woher soll ich wissen ob diese punkte zu strichen werden also manche doppelpunkte werden dann zu / \ - |
bitte einfache antworten die ich verstehen kann.
ps: realschule klasse 10
2 Antworten
Bei einfachen Verbindungen ist die Anzahl der Außenelektronen relevant, die der Nummer der Hauptgruppe entsprechen. Dazu gibt es die OktettRegel, nach der vor allem die NichtmetallAtome der 2. Periode 8 Außenelektronen/4 ElektronenPaare bevorzugen.
Dadurch macht Wasserstoff (fast immer) eine Bindung, die Halogene ebenfalls, Sauerstoff 2, Stickstoff&Phosphor 3, Kohlenstoff 4.
Bei Schwefel und auch Phosphor wird es komplizierter und auch die Halogene, oder Edelgase können auch noch mehr Bindungen eingehen. Aber am Anfang reichen die Faustformeln.
Sauerstoff hat 6 Elektronen. Eine kovalente Bindung vereinnahmt 2 Elektronen, d.h. eines von je einem Bindungspartner. Also könnte Sauerstoff mit seinen 6 Elektronen bis zu 6 Bindungen ausbilden. Solche hohen Mehrfachbindungen treten in der Realität aber aus verschiedenen Gründen nicht auf. Typischerweise bildet Sauerstoff 2 Bindungen aus. Das können sowohl 2 Einfachbindungen zu 2 Bindungspartnern sein, oder aber auch 2 Bindungen zu einem Bindungspartner - das bezeichnet man als Doppelbindung.
Ein Elektron wird mit einem Punkt gekennzeichnet, 2 Elektronen mit einem Strich. Liegt der Strich zwischen 2 Atomen ist damit eine Bindung gemeint (denn die besteht ja aus 2 Elektronen), liegt der Strich direkt am Atom, ist damit ein Elektronenpaar gemeint, also 2 Elektronen, die sich nicht an einer Bindung beteiligen.
Wie viele Bindungen ein Element ausbildet und wie viele Elektronen stattdessen am Element verbleiben, kann man mit fortgeschritteneren Modellen vorhersagen, für den Anfang muss man sich das einfach für jedes Element merken.
Sauerstoff bildet bevorzugt 2 Bindungen aus.
Wasserstoff kann nur eine Bindung ausbilden (es besitzt ja nur ein Elektron).
Kohlenstoff bildet 4 Bindungen aus.
Stickstoff bildet 3 Bindungen aus.
Wichtig ist, dass ein Element nicht mehr Bindungen ausbildet, als es Außenelektronen besitzt. Die Anzahl der Außenelektronen kann an der Hauptgruppennummer abgelesen. Sauerstoff steht in Hauptgruppe 6 - es hat 6 Außenelektronen.
Ein weiteres Hilfsmittel für Elemente aus den frühen Perioden ist die Oktettregel. Sie besagt, dass Elemente 8 Elektronen anstreben. Sauerstoff hat 6 Elektronen. Wenn es 2 kovalente Bindungen ausbildet, kann es sich mit anderen Atomen 2 Elektronen teilen und es hat 8.
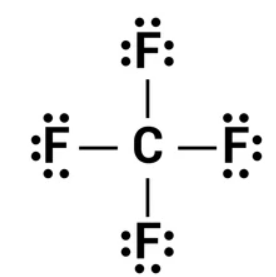
Beispiel: Welches Molekül könnte man aus Kohlenstoff und Fluor bauen? Kohlenstoff steht in der 4. Hauptgruppe, es hat also 4 Außenelektronen. Wenn es 4 kovalente Bindungen ausbildet, ist die Oktettregel erfüllt. Fluor hat 7 Außenelektronen. Für Fluor wäre es gemäß der Oktettregel günstig, wenn es nur eine Bindung ausbildet. Man könnte also ein Kohlenstoffatom mit 4 Fluoratomen über Einfachbindungen verbinden. Das sähe dann so aus:
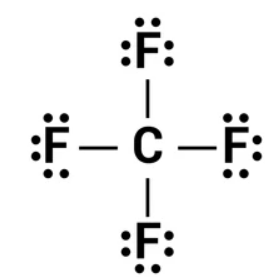
(Hinweis: In dieser Darstellung werden die freien Elektronenpaare an den Fluoratomen nicht durch Striche, sondern durch Doppelpunkte gekennzeichnet)
Sie haben mir keine Frage gestellt. Bitte stellen Sie Fragen öffentlich. So können auch andere Nutzer die Beiträge lesen, die vielleicht ähnliche Fragen haben.
hä tu nicht so auf erwachen ich wollte dich privat fragen und du blockierst mich gleich. ich brauche wirklich hilfe also entblockier mich einfach . ich hab dir privat gesagt ob du mir das mit den punkten und strichen nochmal erklären kannst…
und hör auf mit sie und sag du
Ich habe dich nicht blockiert, ich habe nur wieder die Anfrage aufgehoben. Das ist nicht böse gemeint, aber sag doch einfach hier, was du wissen möchtest. Andere haben vielleicht die gleichen Schwierigkeiten wie du und dann bringt es nichts, wenn man das im Chat bespricht. Was genau verstehst du an den Punkten und Strichen nicht?
ne falls du die regeln hier nicht kennst: kommentare sind dazu da um kleinere kurze gespräche zu führen. und meine frage wird eine disskusion auslösen.
also sei mal normal und wir bereden das privat
und ja jeder hier fragt privat nach und ned in den kommentaren
hä ja danke das du mich blockierst obwohl ich nur eine frage zu dem thema hab, das beweist ja das du die antwort aus dem internet hast, und du in echt 0 ahnung hast.
melde ich gleich erstmal… glückwunsch