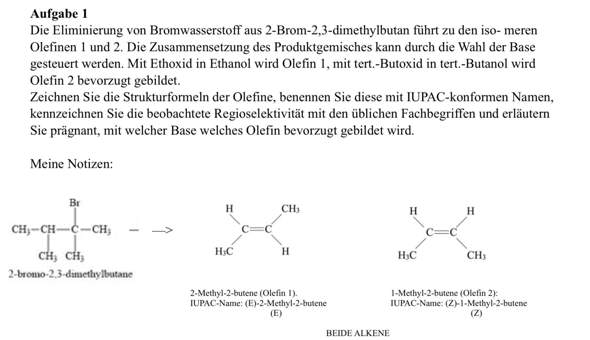
Eliminierung von -HBR aus 2-Brom-2,3-dimethylbutan und Bildung von Olfine 1 und 2?
Hallo gemeinsam, es geht um die Eliminierung von -HBR aus 2-Brom-2,3-dimethylbutan, die zur Bildung von Olfine 1 und 2 führen. Ich habe die entsprechenden Formen rausgesucht und zu verstehen, wie diese entstanden sind, jedoch habe ich einige Probleme damit bzw. Mit dem Prozess der eliminierung und somit die Entstehung der beide Stoffe. Auch mit der Kennzeichnung der Regioselektivität komme ich nicht voran bzw. Weiss nicht was genau gefordert ist..
Demnach bitte ich um eine Erklärung bezüglich diesen und eventuell eine visuelle Darstellung der Problemstellung.
Wäre euch undheimlich dankbar!
Darf ich fragen für welche Klassenstufe bzw Semester die Frage ist.
Ich bin im 2. Semester, aber studiere Chemie nicht, sondern Biologie. Habe es aber als Modul. Hilft es die Aufgabe zu beantworten?
2 Antworten
Die Eliminierung von H-Br erfolgt in trans Stellung, das heißt du musst die dir gauche-Hinderungen entlang der neuen DoBi als Sichtachse vor Augen führen.
Und ist sonst die verlangte Aufgabe richtig?
Nein. Die von dir gezeichneten Moleküle sind falsch und hier geht es um die Regioselektivität der E2 Eliminierung nach den Regeln von Saytzev und Hoffmann.
Nach Saytzev entsteht das 2-Buten als thermodynamisch stabileres Produkt, nach Hoffmann führt die sterisch anspruchsvollere Base zum 1-Buten. Es geht also um das terminale oder interne Alken.
Wenn du die Moleküle richtig malst (2,3-Dimethyl-(XX-)buten) wirst du sehen, daß hier überhaupt kein E oder Z entstehen kann
Ich danke Ihnen für Ihre Antwort, also entsteht von einem 2-Brom-2,3-dimethylbutan ein 2,3-Dimethyl-2-Buten (Olefin1 ) und 2,3-dimethylbutan, richtig? Wo würden sich dann die dopplebildnungen befinden und warum genau?
nein, es entsteht 2,3-Dimethyl-2-Buten und 2,3-Dimethyl-1-Buten
https://www.google.com/search?q=2+3-dimethyl-2-butene
https://www.google.com/search?q=2%2C3-dimethyl-2-buten%2B2%2C3-dimethyl-1-butene
Das 2-Buten ist thermodynamisch stabiler und wird daher nach Saytzev schneller gebildet. Eine sterisch gehinderte Base führt zum 1-Buten.
Im Prinzip geht es hier um thermodynamische und kinetische Reaktionskontrolle. Aber das macht man in der Biologie nicht so ausführlich. Deswegen: einfach noch mal die beiden Regeln googeln.
Vielen lieben dank, aber warum steht da plötzlich H2C? Ich dachte nur, dass die doppelbindung irgendwo anders „bewegt“ wird. Die doppelbindung stellt doch das Entfallen der HBR Bindung, oder nicht? Ich entschuldige mich nochmal für die sämtlichen Fragen, aber ich bin überfordert und wie Sie schon sagten, als Biologie Student ist das auch zu viel für mich..
Weil Kohlenstoff 4bindig ist. Eine Doppelbindung und 2x H
schau dir die Struktur von 1-Buten und 2-Buten an, dann wird es klar.
https://en.wikipedia.org/wiki/1-Butene
https://en.wikipedia.org/wiki/2-Butene
Für deine Reaktion oben spielt das 2,2-Dimethyl vom Verständnis erst mal keine Rolle. Also nehmen wir 2Brom-Butan.
CH3-CH2-CHBr-CH3
Das Brom kann nur eines der beiden dick markierten H für die Eliminierung nehmen und dabei entstehen diese beiden Produkte:
CH3-CH2-CH2=CH2 (terminale DoBi) oder
CH3-CH=CH-CH3 (interne DoBi)
Für die E2 Eliminierung müssen das Br am zweiten C und das H am Nachbar-C anti stehen. Die Steuerung erfolgt über die sterische Hinderung der Base.
Also: kleine, aber starke Base krallt sich das H am dritten C und es entsteht die interne DoBi. Große, sterisch gehinderte Base kommt gar nicht an dieses mittlere C heran und muß daher am terminalen H angreifen. So entsteht die terminale DoBi.
Damit es jetzt nicht unnötig mit E und Z komliziert wird, nimmt man für diese Aufgabe das 2,2-Dimethyl-2Brombutan. Dann kann das nämlich nicht entstehen.
Dankeschön, und wenn man es mit 2-Brom-2,3-Dimethylbutan macht, dann wäre es:
CH3-CH3-CH-CBR-CH3-CH3 (2-Brom-2,3-Dimethylbutan)
und die Eliminierung:
CH3-CH3-CH-CBR-CH3-CH3
CH3-CH3-CH2=CH-CH3-CH3 (intern)
CH3-CH3-CH-Ch2=CH2-CH3 (Terminale)
Mir fiel es wirklich sehr schwere, vor allem weil ich für die 2-Brom-2,3-Dimethylbutan verschiedene Strukturen gesehen habe, habe es auch mithilfe Ihrer gegebenen Formel bisschen rumprobiert, was natürlich falsch und nicht erlaubt ist. Für Korrekturen und Gegenbefehls Erklärungen bin ich natürlich offen und wäre ihnen herzlichen dankbar!
Und kann man anhandessen auch die Anto-Markownikow- Regel und Markownikow- Regel bestimmen? Wenn ja, wäre es in Ihrem fall die terminale DoBi Markownikow- Regel und interne DoBi Anti- Markownikow- Regel, oder?
nein, Markownikow gilt (meines Wissens) nur für die Addition von Halogenwasserstoffen an unsymmetrische Alkene (ohne weitere funktionelle Gruppen).
Anwesender hat darauf hingewiesen, dass die Konformation von Alkanen, hier gestaffelt vs ekliptisch energetisch unterschiedlich ist. Eine Einfachbindung ist dann auch beim Cabenium Ion im Übergangszustand vorhanden ist. Und somit ist eine trans Anordnung wegen der sterischen Hinderung bevorzugt.
Hi LeBonyt,
grundsätzlich ja, aber du hast übersehen, daß die Fragestellerin die beiden Olefine falsch gemalt hat. Wegen "2,2Dimethyl-" gibt es hier kein Cis oder Trans. Es geht nur um die Lager der Doppelbindung nach Hoffmann oder Saytzev.
Ich danke Ihnen für die Antwort! Ansonsten sind die Strukturformel und die jeweiligen Olefine richtig?
Danke für Ihre Antwort! Aber wie soll ich es mit vorstellen? Und ist sonst die verlangte Aufgabe richtig? Außer dass der detaillierter Mechanismus nicht vorhanden ist?