Atomverteilung höhere Perioden?
Hallo wie ist die Verteilung der Atome bei dem Zeichnen des Atombaus. Also ab 4. bis 7. Periode.

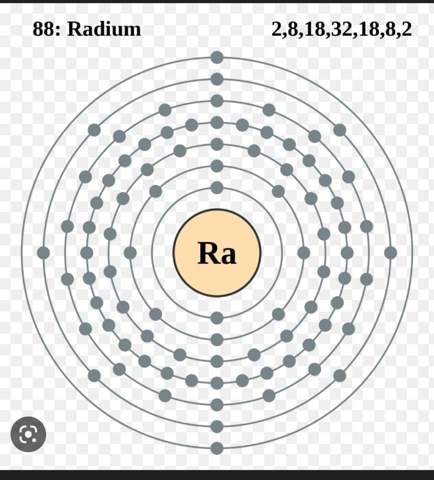
Das habe ich zum Beispiel im Internet gefunden, aber das würde mit dem Bau zum Beispiel auch nicht übereinstimmen
3 Antworten

Schalen gliedern sich in Unterschalen:
- Die s-Unterschale gibt es ab der ersten Schale und sie umfasst ein Orbital mit 2 Elektronen.
- Die p-Unterschale gibt es ab der zweiten Schale und sie umfasst drei Orbitale mit je 2 Elektronen.
- Die d-Unterschale gibt es ab der dritten Schale und sie umfasst fünf Orbitale mit je 2 Elektronen.
- Die f-Unterschale gibt es ab der vierten Schale und sie umfasst sieben Orbitale mit je 2 Elektronen.
Die Auffüllung erfolgt nicht sauber Schale für Schale, sondern nach einem Aufbauprinzip, auch Madelung-Schema genannt. Zu diesem einfachen Schema gibt es, wen wundert's, dann noch Anomalien, die aber wenig interessieren.
Das Aufbauprinzip muss man einmal verstehen und sich einprägen. Aber wenn man es verstanden hat, wird es 1:1 vom Aufbau des Periodensystems widergespiegelt.
Das Bild vom Radium ist übrigens korrekt. Der Text ist etwas problematisch, denn dessen Ansatz versteht man erst, wenn man das Thema verstanden hat. Auch wenn der Text korrekt ist, ist er nur bedingt hildreich.

doch, stimmt alles
1. 2
2. 8
3. 18
4. 32
5. 18 (Minimum bis 32)
6. 8 (Minimum bis 18)
7. 2 (zw. 1-8)

Da gibt es mehrere Möglichkeiten.
Man kann die Elektronenkonfiguration nachschlagen, im PSE, oder bei Wiki. Die wird zwar anders aufgeschrieben, aber man könnte sie abzählen.
Man könnte schauen, wo das Element im PSE steht. In den Hauptgruppen geht die Außenschale von 1-8. Bei den Nebengruppen die 2.-äußerste Schale von 9-18 (mit Ausnahmen). Bei den Lanthaniden und Actinoiden die 3.-äußerste Schale von 19-32.
Die gleichen Grenzen kann man auch als Regel formulieren. Die äußerste Schale trägt höchstens 8, die 2.-äußerste höchstens 18, die 3.-äußerste höchstens 32 Elektronen.

Hö, also wie sich Atome verteilen (als Gas?) hat eher was mit Thermodynamik zu tun, aber nichts mit der Verteilung irgendwelcher Elektronen innerhalb des Atoms.
(Wobei das System mit den Schalen das du da zeigst zum einen nichts mit einer Verteilung von Atomen zu tun hat und andererseits als Modell schon seit ca. 100 Jahren nicht mehr aktuell ist, das nur so als Hinweis)

Das SchalenModell wird in der Schule immer noch benutzt...allerdings wird es eher selten auf die schwereren Elemente angewendet...

Man vermeidet es aus Guten Gründen™, dieses Modell auf schwere Atome anzuwenden. Es ist ja durch keine kompakte Regel beschreibbar, in welche Schale die Elektronen gehen (das gelingt erst, wenn man die Schalen ist s,p,d,f zerteilt).

Ist mir vollkommen klar...weiter als bis zur 4. Periode lohnt sich das auch nicht..
Da kann man noch mal schön die 8 Außenelektronen diskutieren und danach wird es nur noch umständlich und chaotisch.
Aber wie erkenne ich das z.B. bei der 5. und 6. Periode, dass ich es nicht voll also bis zum Maximum 32 bzw. 18 machen muss