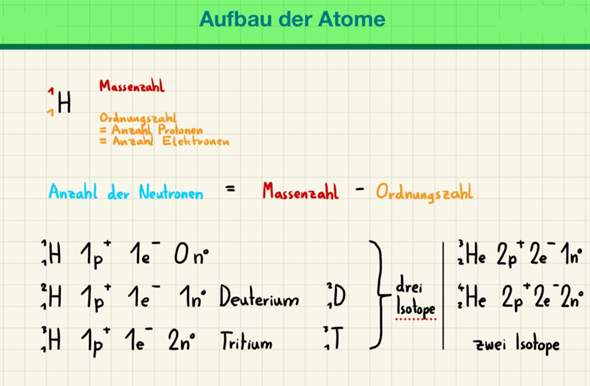
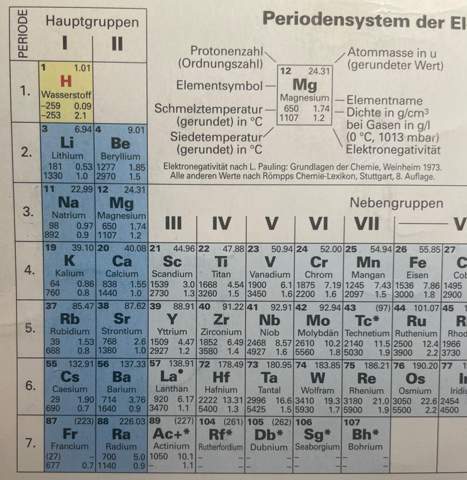
Das rächt sich gerad' so, dass ich "Experimentalphysik 1" letztes Jahr geschoben hab. Denn während meine Kommilitonen sich bereits seit 3 Wochen auf die "Chemie 1"-Klausur vorbereiten, bleibt mir jetzt nur noch die eine Woche (da ich heute noch Ex-Klausur hatte). Da es schnell gehen muss und derzeit jede Sekunde pures Gold ist, verzichte ich auf eine lange Vorleitung und komme direkt zum Punkt. (ok, irgendwie war's dann doch wieder ne lange Einleitung😄)
"Zeichne das Reaktionsdiagramm für
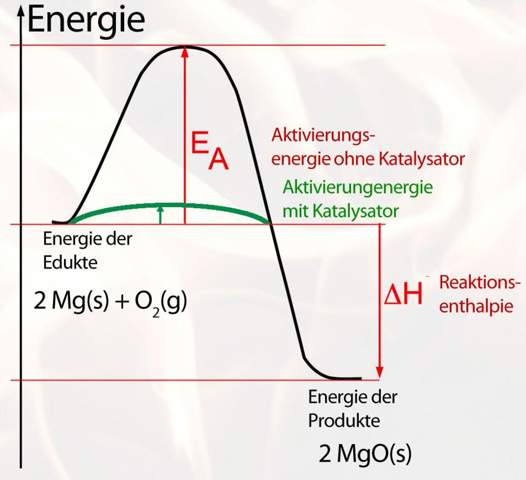
a)eine exotherme Reaktion mit und ohne Katalysator
Stupides Googeln, bzw Allgemeinbildung
(Bildquelle: https://www.u-helmich.de/bio/stoffwechsel/reihe2/Bilder/energiediagrammMgKat.jpg)
b) eine endotherme Reaktion. Zeichne in deiner SKizze die Aktivierungsenergie für die Hin- und Rückreaktion."
Ansatz:
endotherme Reaktion
Jetzt bin ich hier nicht sicher wie ich das der Aktivierungsenergie für die Hin- und Rückreaktion in die Skizze einbringen soll. Ist die Hinreaktion "A2 + X2" und die Rückreaktion "2AX". oder muss ich da noch irgendwas mitreinzeichnen?
Ich weiß dass eine endotherme Reaktion nach dem Motto abläuft, dass die Reaktanden "A-B+C" zu "C-AB" reagieren, also dass quasi die Bindung zwischen A-B aufgebrochen wird und das A zum C gezogen wird. Aber wie soll ich das jetzt graphisch darstellen?
Also es geht mir eigentlich um den Punkt der Aktivierungsnergie für Hin und Rückreaktion.
ich bitte um Verzeihung, wenn es wieder so eine Frage ist, die sich durch stupides Googeln beantworten lässt. Aber ich find da gerad' den Wald vor lauter Bäumen bzw. die Hin/Rückreaktion vor lauter Diagrammen nicht.
Liebe Grüße,
Jensek81