Bei der Hitze sind die Wiesen momentan sehr trocken - nichtzuletzt weil ich auf dem Schlauch stehe:
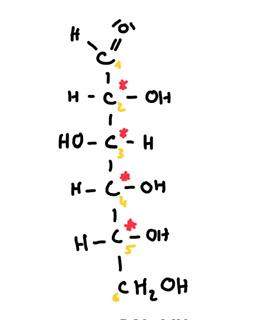
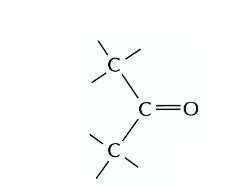
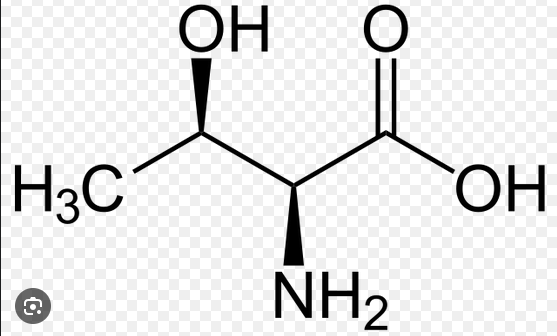
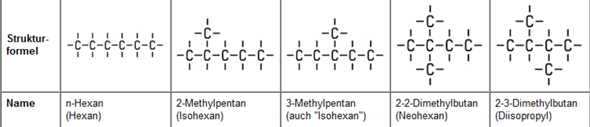
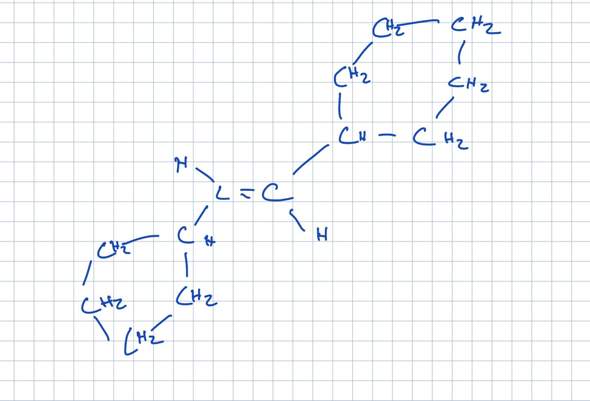
"Zeichnen Sie (2S, 3S)-2-Amino-3-methyl-pentansäure
Ich bin mir nicht sichi wie Siegfried was die (2S, 3S)-Konfiguration angeht. S heißt ja "Gegen-den-Uhrzeigersinn".
Schauen wir uns (3S) an, also die Atome an 3. Stell, von rechts aus betrachtet. Was hängt dort am Kohlenstoff dran.
Über dem Kohlenstoff ist eine CH3-Grupe (gestrichelte Linie).
Links vom Kohlenstoff ist ein C, am welchen zwei H's dranhängen (CH2).
Rechts ist eine C, an welchem zudem noch ein NH2 dranhängt.
Dann hängt zusätzlich noch ein H dran, welches nicht eingezeichnet ist.
Das H bekommt die niedrigste Priorität, also die 4:
Dann haben wir noch CH3, CH2 und CNH2.
Ich hätte jetzt gedacht, daß wir CNH2 die höchste Priorität zu weisen (1), dann CH3 (2) und CH3 (3). Sehe dann so aus.
Das wäre dann, gegen den Uhrzeigersinn, also 3S.
Jetzt hab ich heute mit Kommilitonen drüber diskutiert und die meinten, man muß dem Atom, welches "direkt am Kohlenstoff dranhänge", die Priorität 1 geben. Und das wäre dann das "CH3", weil das eben "unmittelbar am CH3 dranhängt und somit das Wichtigste für uns ist". Stimmt das so? Nicht daß ich irgendjemand anzweifeln möchte, aber das würde für mich zu einem Problem führen. Denn hätte CH3 die Priorität 1, dann hätte CNH2 unweigerlich die Priorität 2 und somit würde der ganze Spaß im Uhrzeigersinn verlaufen, also 3R.
Was? Es ist noch nicht verwirrend genug? Eine Kommilitonin hat das Molekül ein wenig anders gezeichnet - unszwar hat sie das NH2 oben und dafür die CH3 Bindung unten. Also quasi so:
"Heimlich peinlich" denkt sich SpongeBob, denn wenn man jetzt die (R,S)-Konfiguration bestimmen würde, wäre das Ganze wieder gegen den Uhrzeigersinn, nämlich so:
And that makes me ready (Und das macht mich fertig). Denn jetzt wäre das ja wieder gegen den Uhrzeigersinn, also R-konfiguriert.
Kann doch nicht sein, daß wenn ich es so zeichne, es R konfiguriert und ist wenn ich's andersrum zeichen, ist es S konfiguriert. Die Aufgabe geht doch davon aus, dass man im Kopf sofort weiß, wie ich was anordnen muß, damit es S-konfiguriert ist. Ich mache es so wie in der Lösung ganz oben angegeben - halte ich mich an das Schema meiner Kommiltionen ("Das was man angucken will kriegt 1, dann absteigend) und kriege eine R-Konfiguration. Meine Kommilitonin malt das Molekül umgekehrt wie in der Lösung (NH2 oben und CH3 unten) und kriegt aber die gewünschte S-Konfiguration raus.
Je suis verwirrtè en maximal. Peut un person m'aide, s'il vous plait?
LG, Jensek81