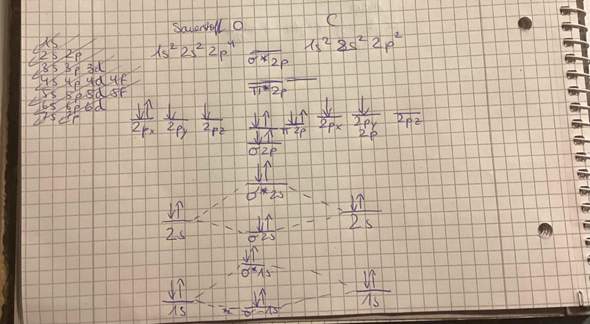
Wie sieht das Molekülorbitaldiagramm aus (C=O)?
Ich versuche gerade, das Zustandekommen des Bürgi-Dunitz Winkels zu verstehen.
Das ist ja der Winkel, (etwa 107 Grad) in dem das Nukleophil zum Beispiel bei einer nukleophilen Addition am Carbonylkohlenstoff angreift. Anscheinend ist es so, dass das HOMO (energetisch höchstes, befülltes Molekülorbital) des Nukleophils Elektronen (meinst auch pi Bindung oder freies Elektronenpaar) ins LUMO des Carbonylkohlenstoffs (in das niedrigste leere Molekülorbital, hier das antibindende pi Molekülorbital) spendet. Damit das HOMO und das LUMO optimal überlappen ist eben der Bürgi Dunitz Winkel notwendig.
So weit so gut. Jedenfalls habe ich versucht, ein Molekülorbitaldiagramm von der C=O Bindung zu zeichnen, aber glaube, dass es falsch ist. Könnte mich da jemand korrigieren? Ich glaube das mit den zwei pi und pi* Molekülorbitalen stimmt nicht ganz.