Lewisformel bei Molekülen?
Hallo,
wie bildet man die Lewisformel von Molekülen. Hier habe ich 2 Beispiele, aber da hat doch jeweils immer nur ein Element 8 Valenzelekrronen. Brauchen nicht alle Stoffe 8 wie zb. bei Beispiel 2 auch Stickstoff?
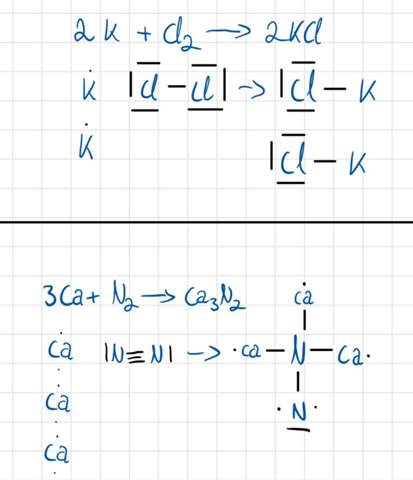
Lg
2 Antworten

Wenn du deine Frage neu einstellst, ändert das nichts daran, dass KCl und Ca₃N₂ Salze sind, Ionenverbindungen. Sie bestehen NICHT aus Molekülen.
Salze bilden ein Ionengitter. Du kannst dir ja mal als Beispiel das NaCl-Gitter ansehen. In dem kristallisieren viele Ionenverbindungen, auch KCl und MgO:
https://de.wikipedia.org/wiki/Natriumchlorid-Struktur

emm...Deine Verbinden sind Salze und für die sind LewisFormeln nicht, oder nur teilweise geeignet! Vor allem gibt es kein BindungsElektronen zwischen den Ionen!
Man kann nur die einzelnen Ionen in LewisFormeln darstellen. Chlorid und Nitrid bildet Ionen mit EdelgasKonfigurationen, also 4 Elektronenpaaren. Die Ionen der 1. und 2. Hauptgruppe haben ebenfalls EdelgasKonfiguration, allerdings das der vorangegangenen Periode! Die eigentliche Außenschale ist leer.

Also kann man davon keine Strukturformel bilden und mein Beispiel ist falsch?