Rechnung chemie?
weiß jemand wie man diese aufgabe berechnet? Das Ergebnis ist 6,9 mL.
Danke
*das Ergebnis ist 6,9 mL
1 Antwort

Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer
Base, Chemieunterricht, Formel
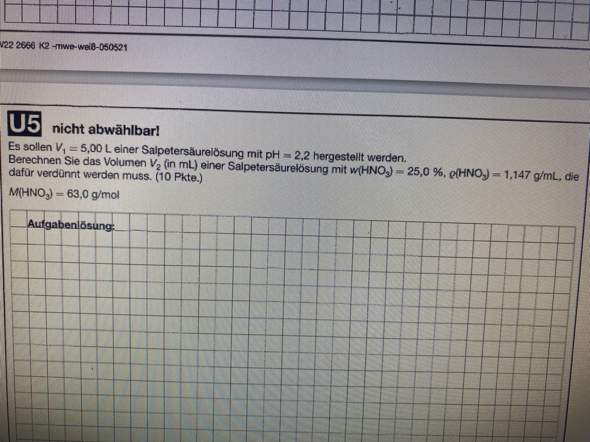
Salpetersäure ist eine starke Säure. Der Zusammenhang zwischen pH und Konzentration lautet daher pH=−lg(c) bzw. c=10¯ᵖᴴ. Wir wollen eine Salpetersäure mit pH=2.2 herstellen, daher soll sie die Stoffmengenkonzentration c=10¯²·²=0.0063 mol/l haben.
Das herzustellende Volumen beträgt V=5 l, also brauchen wir 0.032 mol HNO₃. Als Ausgangslösung steht eine Salpetersäure w=25% und ρ=1.147 g/ml zur Verfügung. Ein Milliliter davon wiegt Vρ=1.147 g, und davon sind 25% also 0.287 g reine HNO₃, das entspricht n=m/M=0.00455 mol. Daher brauchen wir 0.032/0.00455=6.93 ml davon.