Mesomere Grenzstrukturen des intermediären σ-Komplexes?
"Er ist wieder voll in seinem Element"
Wir verstehen gerade nicht so ganz, wie viele mesomere Grenzstrukturen es bei der Sulfonierung von Thiophen in Position 3 ("meta zum Schwefel") gibt. Und unser Dozent ist sich leider selber nicht so sichi wie Siegfried.
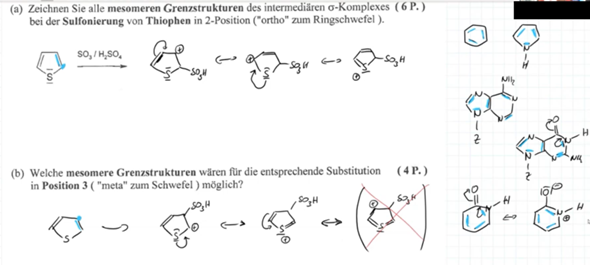
Ist das ganz unten rechts (was rot durchgestrichen ist) ebenfalls noch eine mesomere Grenzstruktur? Wir sind uns gerade nicht sicher wie wir die Striche über dem S interpretieren sollen? Ist das 'ne Doppelbindung oder sollen das Außenelektronen sein? Schwefel hat ja 6 Außenelektronen, also braucht es noch 2 um die Edelgaskonfiguration zu erreichen. Aber ein Strichlein bedeutet ja immer ein Elektronenpaar, also genügt da doch eigentlich ein Strich bei dem S und nicht zwei Striche (das wären dann ja 4).
Sind das dann gar keine Außenelektronen, sondern Doppelbindungen? Weil dann wäre das durchgestrichene ja keine mesomere Grenzstruktur? Oder ist es doch eins?
1 Antwort
Die letzte mesomere Struktur ist zu Recht durchgestrichen. Einfach deshalb weil Schwefel da (formal) 5 Bindungen hat, was ohne Mehrzentrenbindungen schlicht nicht geht. Da sind 2 Doppelbindungen auf jeder Seite, die schon jeweils 2 Orbitale brauchen. Und dann habt ihr da auch noch das freie Elektronenpaar, das ja auch irgendwo rein muss.
Zumal zwei Doppelbindungen in so einem Winkel ja sowieso eher ungünstig sind.
Meinst du beim Thiophen? Naja, für die Oktettregel braucht Schwefel 8 Außenelektronen, das stimmt. Die hat es auch. Nämlich je 2 von den beiden freien Elektronenpaaren (die Striche über und unter dem S) und je 2 aus den beiden Bindungen zu den Kohlenstoffatomen. Macht insgesamt 8.
Die 6 Außenelektronen, die es im ungebundenen Zustand hat, sind für das Zählen der Elektronen in einer Verbindung unerheblich.
Ja, aber ich dachte ein Strich steht für 2 Elektronen.
Wenn S zwei freie Elektronen hat, dann müsste da doch eigentlich nur ein Strichlein hin.
Vor allem ist die Oktettregel alles andere als brauchbar, wenn es um Elemente geht, die Zugang zu d-Orbitalen hat
S hat zwei freie Elektronenpaare, also 4 Elektronen. Sonst würdest du ja auch nicht auf insgesamt 8 kommen mit denen aus den Bindungen.
d-Orbitale sind bei Schwefel doch irrelevant. Dass es da d-Orbital Beteiligung hat man mal gedacht, aber wurde widerlegt.
Ich habe mich auch nicht auf Schwefel bezogen :-) hab ich nirgendwo geschrieben
Dann versteh ich nicht worauf das bezogen war
Ok, danke für die Antwort. Aber was ich jetzt nicht verstehe: Schwefel hat doch 6 Außenelektronen - braucht also nur noch 2 um nach Okettetregel die Edelgaskonfiguration zu erreichen. Warum malt man dann einen Strich über dem S und einen unter dem S. EIn Strich steht doch immer für 2 Elektronen (= 1 Elektronenpaar): Der Logik zufolge hätte das S ja jetzt 4 Außenelektronen (= 2 Elektronenpaare). Und das ergibt für mich kein Sinn