Frage Franck Hertz Versuch?
Hallo, ich habe eine Frage zum Franck Hertz Versuch und zwar, wieso wandert der Leuchtstreifen, also der Streifen an dem die Ag-Atome angeregt werden mit der Zeit zur Kathode?
Und noch eine dumme Frage: Wieso gewinnen die Elektronen überhaupt an Energie im Laufe ihres Weges zu dem Gitter und haben nicht immer die gleiche Energie?
Vielen Dank im Voraus für Antworten und ich hoffe man versteht was ich meine.
Hallo, also mir ist jetzt selbst die Antwort eingefallen:
Die Elektronen gewinnen an Energie weil sie ja beschleunigt werden und dadurch nimmt v immer zu. Für die kinetische Energie gilt ja: E=1/2 mv^2, d.h die kinetische Energie nimmt immer weiter zu. (Ich frage mich da nur noch wie das mit dem Energieerhaltungssatz vereinigbar ist)
Der Leuchststreifen bzw. die Absorbtionsschicht wandert zur Kathode, weil die Beschleunigungsspannung ja immer weiter erhöht wird, dadurch haben die Elektronen schon "früher" genug Energie, um die Hg-Atome anzuregen und der Leuchtsstreifen wandert nach vorne.
Ich hoffe ich hab das jetzt richtig verstanden :)
1 Antwort
Schau Dir mal die vereinfachte Simulation hier an: https://www.leifiphysik.de/atomphysik/atomarer-energieaustausch/versuche/franck-hertz-versuch-mit-hg
Wieso gewinnen die Elektronen überhaupt an Energie im Laufe ihres Weges zu dem Gitter
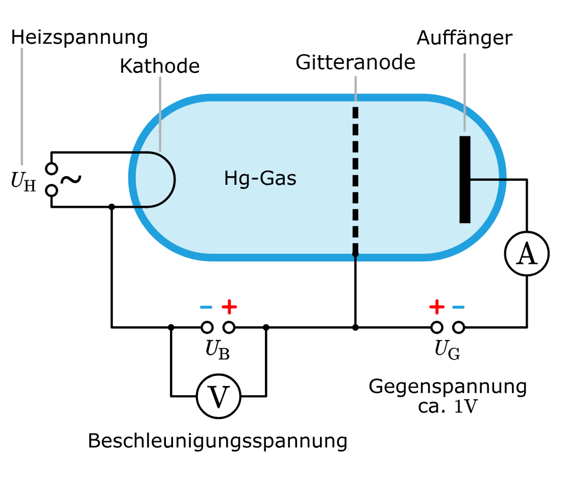
Zwischen Kathode und Gitteranode ist eine Spannung (Beschleunigungsspannung) und Elektronen werden im elektrischen Feld entsprechend F = q·E = m·a (q = -e) beschleunigt. Da die Gitteranode positiv geladen ist, werden die negativ geladenen Elektronen in Richtung Gitteranode beschleunigt.
Und damit zur ersten Frage:
wieso wandert der Leuchtstreifen, also der Streifen an dem die Ag-Atome angeregt werden mit der Zeit zur Kathode?
Weil bei einer wechselnden Beschleunigungsspannung nach unterschiedlichen Strecken den Elektronen genügend kinetische Energie zur Verfügung steht, die bei einem Stoß mit den Hg-Atomen zu einer Anregung derselben führen kann. Wie in der oben verlinkten Simulation zu sehen ist, kann man durch Erhöhung der Beschleunigungsspannung den Elektronen so viel kinetische Energie zuführen, dass diese dazu reicht, den Prozess der Anregung von Hg-Atomen mehrmals in Gang zu setzen, sodass mehrere Leuchtstreifen erscheinen.