3 universelle Gasgleichungen?
Gibt es 3 universelle Gasgleichungen?
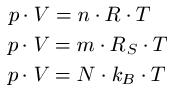
Und muss man sich das so vorstellen, dass
n * R = m * R_S = N * k_B
Aber warum ist das denn alles gleich?
2 Antworten

Gibt es 3 universelle Gasgleichungen?
Nein. Es gibt nur eine universelle Gasgleichung, die Èmile Clapeyron aus dem Gesetz von Guy-Lussac sowie dem Gesetz von Mariotte mathematisch herleitete.
Veröffentlicht wurde sie erstmal 1834 und lautet im Original:
pv = R(267 + t)
t war dabei die Celsiustemperatur und (267 + t) wird heute die absolute Temperatur T genannt. Damals kannte man den absoluten Nullpunkt von -273,15 °C aber noch nicht genauer.
R war in diesem Fall die spezifische Gaskonstante, bezogen auf die Masse m.
v ist das spezifische Volumen, also V/m
Alle weiteren Formulierungen wurden später aus dieser Grundformel hergeleitet. So wurde die Boltzmannkonstante, die absolute Gaskonstante oder der absolute Nullpunkt erst nach Clapeyron "entdeckt".

p = Druck
V = Volumen
T = absolute Temperatur
n = Stoffmenge in mol
R = universelle Gaskonstante (8,314 J/(mol×K)
kb = Bolzmankonstante ist wie R, nur für ein Teilchen, also kb=R/n. Statt der Stoffmenge nimmt man dann die Teilchenzahl N.
m = Masse. Um die direkt zu verwenden nimmt man eine spezifische Gaskonstante Rs. Da m=n×M (Molmasse in g/mol) ist Rs=R/M (in J/(kg×K)