Wie berechnet man den Pufferbereich?

1 Antwort
Du rührst einen symmetrischen Puffer zusammen, der je 10 mmol NH₃ und NH₄⁺ in 100 ml enthält. Der pH beträgt pH=pKₐ=9.25.
Bei Zugabe von V=9 ml einer c=1 mol/l HCl kommen n=cV=9 mmol HCl dazu, die ebensoviel NH₃ zu NH₄⁺ protoniert, also haben wir dann 1 mmol NH₃ übrig, und insgesamt 19 mmol NH₄⁺. Die Henderson–Hasselbalch-Gleichung sagt eine Verschiebung des pH um lg(NH₃/NH₄⁺) voraus, das sind lg(1/19)=−1.28 pH-Einheiten zu 7.97.
Mit der NaOH ist es genauso nur umgekehrt, also erwartet man einen pH=pKₐ+lg(NH₃/NH₄⁺)=4.25+1.28=10.53.
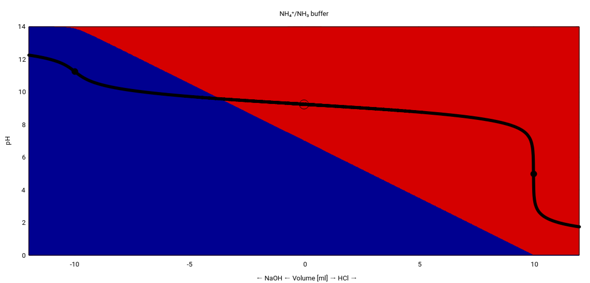
In dieser Graphik siehst Du das Verhalten genauer. Der x-Wert 0 gehört zum Ausgangspuffer, und zu negativen Werten siehst Du den pH bei Laugenzugabe, zu positiven den bei Säurezugabe.
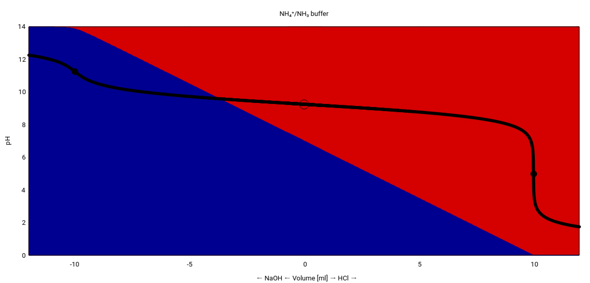
Außerdem zeigen die Hintergrundfarben die Mengen NH₄⁺ (rot) und NH₃ (blau) an. Du siehst, daß der Puffer überlastet ist, wenn das zugetropfte Volumen Säure bzw. Base 10 ml erreicht, denn dann ist jeweils eine Komponente des Puffers aufgebraucht.