Oxidationszahlen von Ameisensäure?
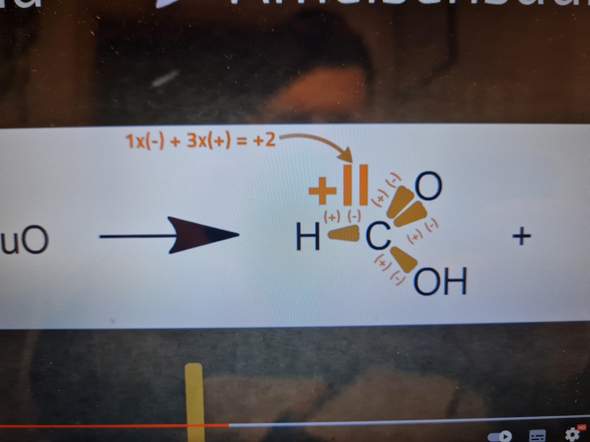
Moin versuche Redoxgleichungen zu Üben nun habe ich mir Ein Video Angeschaut indem bei der Reaktion Ameisensäure die gesamt Oxidationszahl +2 hat aber egal wie ich es drehe und wende ich komme nicht auf +2 kann mir da vielleicht jemand Helfen?
Lg
3 Antworten
Naja, um die Oxidationszahl zu bestimmen, gehst du wie folgt vor:
Du schaust dir zunächst an was das fragliche Atom (also das C) für Bindungspartner hat. Ist der Partner nun elektronegativer (wie das O) bekommt er die Elektronen aus der Bindung mit dem C. Ist er elektropositiver (wie das H) dann erhält das C die Elektronen aus der Bindung. Hier verliert das C also alle Elektronen in Bindungen mit Os und gewinnt die aus der Bindung mit dem H. Es hat also 2 Elektronen.
Jetzt schaust du dir an, wie viele (Valenz)Elektronen das C im elementaren Zustand bzw "ungebundenen" Zustand hat (Das ist die Gruppennummer im Periodensystem). Das wären 4.
Und zuletzt ziehst du diese beiden voneinander ab: 4 - 2 = 2
Ok, edit: hatte das - vor der 2 in deiner Formel nicht gesehen. Dann ist sie natürlich falsch.
Es geht um die Oxidationszahl des C-Atoms. Dazu wird verglichen, wie viele Bindungen er zu Atomen hat, die elektronegativer sind als er selber und zu wie vielen, die elektropositiver sind.
Das ist auf dem Bild dargestellt. H ist positiver als C. Dafür bekommt er also 1x "-".
Zu Sauerstoff (O) hat er insgesant drei Bindungen. Sauerstoff ist elektronegativer als C. Dafür gibt es also 3x "+". Jetzt nur zusammen rechnen: 3 + (-1) = 2
Die Sache mit negativen Zahlen ist klar? Man kann auch schreiben:
-1 + 3 = 2
hmm, da sind 3 oxidative Bindungen (zu Sauerstoff) und eine reduktive (zu Wasserstoff). Ergibt zusammen 2 oxidative (= +II).
Dann habe ich wahrscheinlich einen Denkfehler weil ich dachte die Formel wäre dann 4 e- - -2 e- = -2