Wie kann dieses Molekül zustandekommen (H3PO4)?
Die Rede ist vom Molekül oben links. Ich verstehe ja, dass das passt von der Anzahl der Valenzelektronen, aber aber wie kann Sauerstoff mit den Valenzelektronen eine Bindung eingehen, die normalerweise am P kleben (sorry, weiß die Namen davon nicht), also die gleiche Art von Elektronen, wie die eingekreisten von dem Rechten Molekül? Und hat das P dann nicht zu viele Elektronen? Und abgesehen von dem unteren Molekül, das es eigentlich nicht gibt, ich dachte auch immer, dass drei EP am Chlor kleben müssen, aber wenn das mit dem Phosphor klappt, müsste dann nicht auch von den Elektronen her sowas wie im unterm Bild klappen? Oder ist bei dem Phosphorm
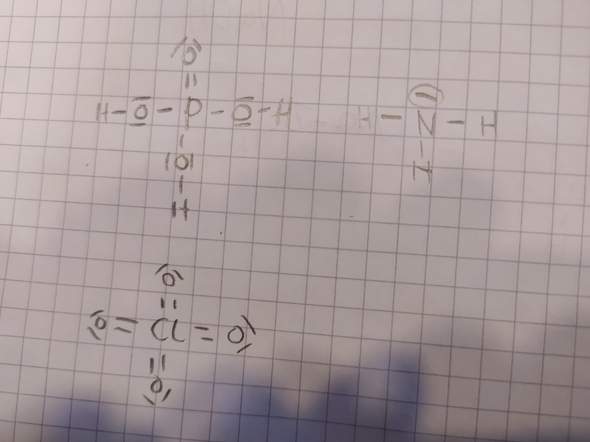
olekül etwas anders?
Also ich meine bei dem CL Molekül nur drei doppelbindungen, und bei der anderen Wasserstoff statt Sauerstoff, also dass die drei elektronenpaare, die normalerweise am Chlor kleben, für Bindungen verwendet werden, wie bei dem oben links
2 Antworten
Stimmt schon, die Elektronen "kleben" normalerweise am Phosphor. Wenn aber dann ein Atom mit hoher Elektronegativität daherkommt (wie zum Beispiel Sauerstoff), dann ist dieses in der Lage dem Phosphor seine Elektronen zu entreißen.
Wie dir ja bekannt sein dürfte, streben alle Elemente immer nach dem Elektronenoktett (bzw einer vollen Schale). Das machen sie durch Elektronenaufnahme oder -abgabe. Elemente wie Stickstoff und vor allem Sauerstoff und Fluor nehmen wegen ihrer hohen Elektronegativität quasi immer Elektronen auf. Jetzt sollte man vielleicht meinen das wäre bei Phosphor auch so, weil es ja unter N steht. Das ist aber nicht so. Ein Phosphoratom ist größer und weniger elektronegativ als Stickstoff, das führt dazu, dass es seine Elektronen schlechter festhalten kann. Deswegen kann Sauerstoff ihm die auch abziehen.
Um sein Elektronenoktett trotzdem zu erreichen muss Phosphor dann alle seine äußeren Elektronen (5 an der Zahl) abgeben, also 5 Bindungen mit Sauerstoff eingehen. Das führt dann letztendlich zu H3PO4.
Übrigens gibt es diese Chlorverbindung fast so, wie du sie da aufgemalt hast. Es ist nur eine Bindung zu viel. Chlor hat ja 7 Valenzelektronen, die es alle abgeben müsste, also 7 Bindungen. Ergibt das hier: https://de.wikipedia.org/wiki/Perchlorsäure
Chlordioxid gibt es durchaus: https://de.wikipedia.org/wiki/Chlordioxid . Drei Doppelbindungen sind theoretisch möglich, aber energetisch so ungünstig, dass es sofort wieder zerfällt.
Bei Phosphor ist das mit seinen 5 Außenelektronen anders. Welche Molekülorbitale stabil sind, also energetisch günstig, und welche schnell wieder zerfallen, wobei Energie frei wird, liegt an der Quantenmechanik. Die Berechnungen dafür sind schwierig und umfangreich, aber experimentell lässt sich das leicht bestimmen.