Valenzschale Chemie?
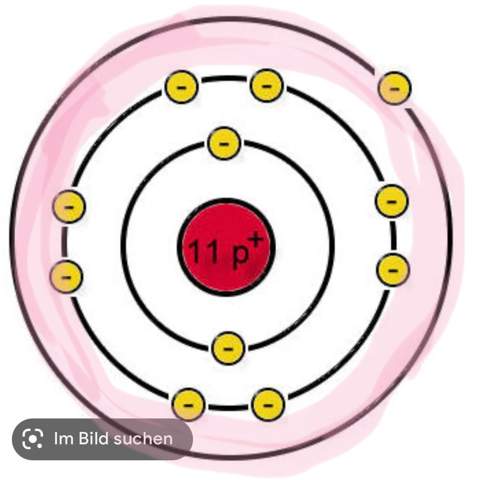
Hi, ich hätte mal eine Frage an die Chemiker. Das, was ich so rosa markiert habe, ist das die Valenzschale. Das ganze Ding zusammen nennt sich Atom und in der Mitte, das ist der Atomkern und die gelben sind die Elektronen, oder?
2 Antworten

Moin,
ja, das hast du richtig verstanden.
Ein Atom besteht aus einem Kern und einer Hülle (Kern-Hülle-Modell).
Im Kern findest du die positiv geladenen Protonen (und - bis auf Wasserstoff - auch immer die ungeladenen Neutronen) Das siehst du in deiner Darstellung als „p+”. Das „p” steht für Proton und das „+” für die Ladung dieses Atombausteins.
Die Hülle ist nun ihrerseits auch noch einmal strukturiert. In deiner Darstellung (Schalenmodell) siehst du Kreisbahnen um den Atomkern. Auf diesen Kreisbahnen befinden sich in der Hülle die negativ geladenen Elektronen („e–”). Die sind in deinem Bild jedoch durch die gelben Kreise mit dem Minuszeichen darin dargestellt.
Die innerste (kleinste) Schale kann dabei maximal zwei Elektronen aufnehmen (was sie in deiner Darstellung ja auch macht). Die nächste Schale hat dann Platz für maximal acht Elektronen (was ebenfalls gegeben ist). Die darauf folgende Schale hätte nun zunächst wieder für acht Elektronen Platz (in Wirklichkeit könnte sie insgesamt 18 Elektronen aufnehmen, aber zehn Elektronen werden erst in diese Schale gezwängt, wenn auch Elektronen in der nächsten, der vierten Schale untergebracht worden sind; das hat etwas mit der Feinstruktur und der Energie der Schalen zu tun, aber das kann man erst verstehen, wenn man ein anderes Atommodell - das Orbitalmodell - kennengelernt hat. Das soll uns hier erst einmal nicht weiter interessieren und belasten).
Okay, obwohl in der dritten Schale also zunächst auch wieder Platz für acht Elektronen wäre, befindet sich in deiner Darstellung dort nur ein einziges Elektron. Das kommt daher, dass du im Kern dieses Atoms nur elf Protonen hattest.
Da ein Atom per Definition nach außen ungeladen ist, müssen diese elf positiv geladenen Protonen genau so viele negativ geladenen Gegenladungen haben, was in einem Atom die Elektronen übernehmen. Darum stehen den elf positiv geladenen Protonen im Kern auch elf negativ geladene Elektronen in der Hülle gegenüber, weil sich so die Wirkung der elf Plusladungen und die Wirkung der elf Minusladungen gegenseitig aufheben: das Atom erscheint nach außen hin ungeladen (obwohl es aus verschieden geladenen Teilchen zusammengesetzt ist).
Tja, aber wenn auf der innersten Kreisbahn (der K-Schale) zwei Elektronen und auf der nächsten Kreisbahn (der L-Schale) acht Elektronen sind, dann hast du von deinen elf Elektronen bereits zehn verteilt. Das bedeutet, dass für die letzte Kreisbahn nur noch ein Elektron übrig bleibt (obwohl dort mehr Elektronen Platz hätten). Und genau das siehst du in deiner Darstellung.
Na ja, und weil also die dritte Kreisbahn die letzte ist, auf der es noch Elektronen gibt, bildet diese Schale in diesem Atom die Außenschale.
Die Elektronen der Außenschale nennt man folglich auch Außenelektronen oder auf schlau Valenzelektronen. Der Begriff Valenzelektronen enthält das Wort „valent” oder „Valenz”, was so viel wie „Wert” bedeutet. Das kommt daher, dass bei chemischen Bindungen fast immer nur solche Außenelektronen von Bedeutung sind, so dass nur sie für das Zustandekommen von Bindungen einen Wert haben, verstehst du?
Die anderen, weiter innen liegenden Elektronen bezeichnet man als Rumpfelektronen, weil sie zusammen mit dem Atomkern den Atomrumpf bilden.
Du siehst, du hast alles richtig verstanden...
LG von der Waterkant

Dankeschön für die ausführliche Antwort. Ich habe jetzt alles verstanden.

stimmt!
Das ist natürlich ein sehr (!) einfaches Modell eines Atoms, aber einfach zu verstehen...