Oxidationszahlen?
Halli Hallo
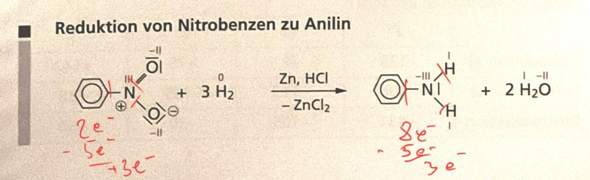
könnte mir bitte jemand erklären, wie bei Nitrobenzol die Oxidationszahl von Stickstoffatom auf +III kommt und bei Anilin auf -III.. Soweit ich gelernt habe sollte das Stickstoffatom von Aminogruppe auf -II kommen, den wir haben nur zwei Wasserstoffatome.
vielen Dank im Voraus

2 Antworten
Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer
Chemieunterricht, Oxidation, Redoxreaktion
Stickstoff ist elektronegativer als C.
- In der Nitrogruppe bekommt der N die beiden Elektronen aus der CN-Bindung zugeteilt, aber sonst nichts, weil O elektronegativer als N ist. Er hat also 2 Elektronen bzw. Oxidationszahl +III.
- In der Aminogruppe ist der N nur an elektropositivere Atome gebunden und hat außerdem noch ein lone pair. Das macht 8 Elektronen bzw. Oxidationszahl −III.
Von
Experte
indiachinacook
bestätigt
Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer
Chemieunterricht, Redoxreaktion, Reaktionsgleichung
Stickstoff hat eine höhere Elektronegativität als Kohlenstoff, aber eine niedrigere als Sauerstoff. Entsprechend kann man die Elektronenpaare zuweisen und dann die Ladung abzählen!