Warum ist NCl3 explosiv und instabil?
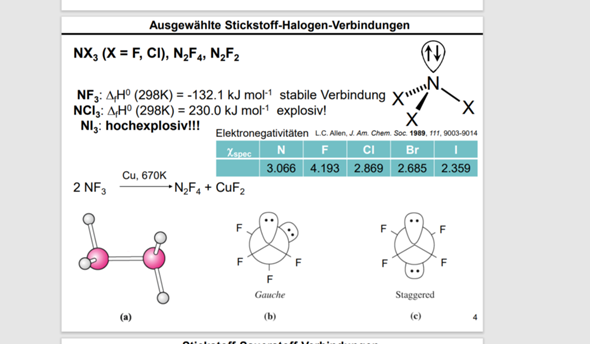
Ich verstehe das das N in NF3 positiv polarisiert ist gemäss den spektroskopischen Elektronegativäten in der türkisen Tabelle, und das N in NCl3 stark negativ polarisiert ist.
Warum ist das so instabil und steigert sich bei NI3?
Danke :)
2 Antworten
Wie schon erwähnt ist die Elektronegativität nur ein ganz grobes Hilfsmittel. Später im Studium in der PC lernt man auch, weshalb. Ich versuche es kurz und grob zu erklären.
- Man kann mittlerweile die Elektronendichteverteilung und Orbitalenergien numerisch gut berechnen. Sehr abweichende Radien und ENs bedingen manchmal ungünstigen Überlapp der Atomorbitale, schlechte Gitterenergien oder sterische Hinderung (hier erstes und letztes).
- Geringe Aktivierungsenergie, Autokatalyse oder eine ähnliche Triebkraft wäre möglich. Zumindest entropisch ist NI3 sehr ungünstig; energetisch?!
- Je nach Verbindung, Hybridisierung und formaler Oxidationsstufe kann man einem Element oder sogar ganzen Atomgruppen verschiedene Elektronegativitäten zuschreiben (bspw. -CF3: 3,1). Die EN ist unterschiedlich definierbar nach Pauling, Rochow, Mulliken...
- (Kinetische) Stabilität gegenüber Wasser und O2 ist zumindest bei den ÜG-Metallkomplexen entscheidender als die schwachen Bindungsenergien mit den d-Orbitalen.
Zusammenfassend: Fluor ist schön klein, liebt Elektronen und hat im MO-Schema einen hohen Energiegewinn (N, F: ähnliche EN und Radien), Iod ist ein fauler Riese, wird leicht rausgekickt und N2-Dreifachbindung und Entropie machen NI3 instabil.
PS: Was sind spektroskopische Elektronegativitäten? Sind die aus UV-Vis-, XPS- und UPS-Spektren, oder Elektronenspektren?
PPS: Die Annahme, dass Atome immer Edelgaskonfiguration (N: +5/-3) erreichen "wollen", ist eine zu starke Vereinfachung des EN-Konzeptes.
Es lässt sich nicht alles mit Elektronegativität erklären. Das N₂-Molekül hat einfach eine enorm hohe Bindungsenergie.
Frag mich nach Gründen, warum die Dreifachbindung gerade beim Stickstoff so stabil ist, und ich werfe das Handtuch.
Es ist jedoch Fakt. Auch Na₃N ist aus diesem Grunde instabil.
Dass die Atome in der gleichen Periode stehen, hat auch einen erheblichen Einfluss. Qualitativ betrachtet funktioniert die Überlappung der Orbitale besser.
Irgendeine Idee warum dann NF3 stabil ist?