Sollte NH2(CH3)2 in einer Reaktion nicht eher als Radikal reagieren als ein schwaches Nucleophil einer SN1-Reaktion?
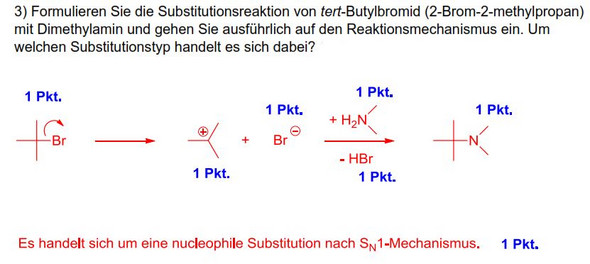
Ich verstehe nicht ganz, wieso das Amin plötzlich zwei H-Atome trägt. Stickstoff besitzt 5 Valenzelektronen, durch die Bindung mit einem H-Atom und einer CH3-Gruppe sollte es doch die Edelgaskonfiguration erreicht haben, mit den 10 Elektronen. Müsste dann nicht NH2(CH3)2 ein Radikal sein? Damit wäre es ja keine SN1-Reaktion mehr sondern eher eine radikalische Substitution. Oder hat es irgendwas mit Hyperkonjugation zu tun? Wo liegt mein Denkfehler?
5 Antworten
Amine können nucleophil an einem Kation angreifen, da sie ein nicht bindendes Elektronenpaar besitzen. Bei Dimethylammonium [NH2(CH3)2]+ befindet sich am Stickstoff eine positive Ladung, ein nucleophiler Angriff ist nicht mehr möglich.
Stickstoff hat mit 3 Bindungen (3 x 2 Elektronen) + 1 nicht bindenden Elektronenpaar 8 Valenzelektronen und die Oktettregel erfüllt (3 halbe Elektronenpaare + ein nicht bindendes = 5 Valenzelektronen)
Ich halte das für einen Fehler in der Angabe. Wie hier schon ein paar Leute gesagt haben: Diemthylamin ist NH(CH₃)₂ und ein Nuclephil, daß in diesem Fall nach SN1 glatt reagieriern sollte. Es kann auch ein Proton aufnehmen und zu NH₂(CH₃)₂⁺ (Diemthylammonium) werden, aber in dieser Form ist es kein Nukeophil mehr.
Ein neutrales Teilchen NH₂(CH₃)₂ gibt es nicht — es müßte ein Radikal sein, hat aber bereits gefüllte 2s und 2p Orbitale am Stickstoff, also keinen Platz für ein Extra-Elektron. Deshalb gibt es auch kein neutrales NH₄ (außer als Amalgam, wo das überschüssige Elektron ans Leitungsband des Quecksilbers abgegeben wird), oder vielleicht als Rydberg-Zustand in der Gasphase.
Sollten hier nicht rechtzeitig fachkundige Nutzer auftauchen, versuch es doch mal in einem Fachforum: http://www.chemieonline.de/forum/
Es gibt natürlich ein Dimethylammonium-Kation, also ein protoniertes Dimethylamin, das hat dann aber eine positive Ladung und ist somit nicht geeignet ein (positives) Carbeniumion nucleophil anzugreifen. Die Darstellung von Dimethylamin ist also fehlerhaft.
Ich denke mal, dass das ein Tippfehler ist und dass einfach Dimethylamin gemeint ist. Dessen Summenformel ist NH(CH3)2.
Das Endprodukt hat ja auch kein Wasserstoff mehr am Stickstoff und es wird nur ein Equivalent an Wasserstoff entfernt.
Das freie Elektronenpaar des Stickstoffs reagiert dann mit dem Carbokation, das verbliebene Proton am Stickstoff wird abgespalten und der entstehende Bromwasserstoff verdampft.
Stimme ich zu. Bei den Produkten fehlt nämlich auch dieses eine ominöse H.
Edit: in der Angabe steht ja sogar, dass Dimethylamin verwendet wird. Das hat mit Sicherheit nur ein Wasserstoffatom am Stickstoff gebunden.
Ok, danke! Ich war mir nur unsicher, ob es dazwischen nicht noch eine Reaktion mit dem Dimethylamin gegeben hat.