Erwärmungsdiagramm von Wasser?
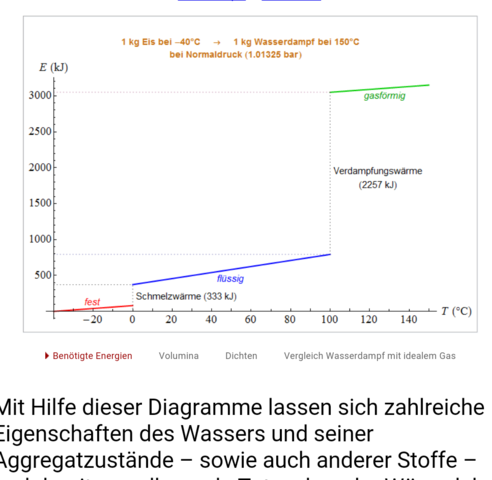
Hi :) Ich habe ein Bild beigefügt. Was ich nicht ganz verstehe ist, dass in den Abschnitten wo die Temperatur konstant ist beide Phasen zugegen sind. Wie kann das denn sein, dass es Wasserdampf und flüssiges Wasser gleichzeitig geben kann? Hilfe! Vielen Dank :))
4 Antworten

Das ist das physikalische Äquivalent der "Disproportionierung".
Gas und Flüssigkeit nebeneinander haben eine kleinere Enthalpie als das hypothetische Fluid dazwischen.

Es gibt immer flüssiges und gasförmiges Wasser nebeneinander.
Solange es flüssiges Wasser gibt.
Die Luft um dich ist nie ohne Wasserdampf.
Solche Sachen begreift man ganz praktisch, wenn man sich sein Essen - und nachher seine eisgekühlten Drinks - selbst zubereitet.
Oder sich sein selbstgekauftes Tiefkühlessen kocht.

Hast du schonmal Wasser gekocht? Was passiert denn da? Verdampft das Wasser schlagartig zu Wasserdampf oder hast du vielleicht zu irgendeinem Zeitpunkt Wasserdampf über dem Topf und Wasser im Topf? ;)


Deine Frage ist aber aus deinem Diagramm nicht ersichtlich.
Wenn du en Tripelpunkt des Wasser meinst, dann sieht das Diagramm wie in folgenden Link aus.