Chemie woran erkennt man Redoxreaktionen?
Hi ich hab mir jetzt schon ein paar Videos angeguckt aber ich checke nicht woran man erkennt, dass eine Redoxreaktion möglich ist... könnt ihr mir es versuchen zu erklären? 😬
1 Antwort
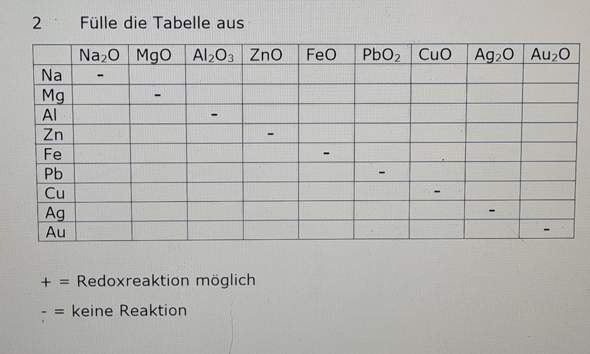
Hier ist eine Tabelle, in der verschiedene Metalle nach ihrem "Redoxpotential" sortiert sind.
- Je edler, desto weiter oben steht das Metall.
- Je unedler, desto weiter unten steht das Metall.
Wahrscheinlich hast du so eine Auflistung auch in deinem Schulbuch.
https://de.wikipedia.org/wiki/Elektrochemische_Spannungsreihe?wprov=sfla1
------------------------------------------------------------------------
Merke: Eine Redoxreaktion läuft nur ab, wenn der Sauerstoff am unedleren Metall gebunden ist. Oder wenn wir es auf die Tabelle beziehen: Sauerstoff kann nur "runterfallen".
Jetzt gucken wir uns ein Feld an - z.B. oben links: Mg + Na2O
Mg ist edler als Na. Deswegen läuft diese Reaktion NICHT ab.
Anders formuliert: Der Sauerstoff müsste vom Na zum Mg "hochfallen". Das geht nicht.
Alles klar?