Warum greifen Elektronenschalen ineinander?
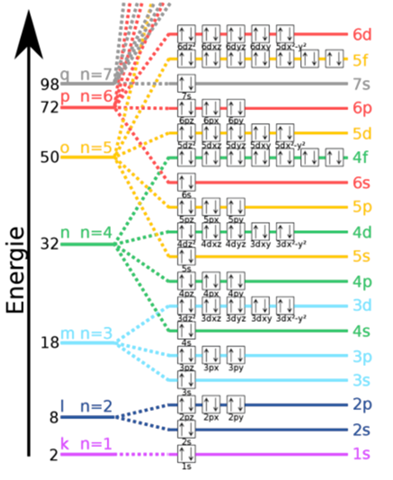
Warum greifen die Elektronenschalen ineinander, sodass Elektronen einer niedrigeren Schale ein höheres Energieniveau als Elektronen einer höheren Schale haben können ? (Wie 5s, 4f, ...)
1 Antwort
Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer
Chemie, Atom, Elemente
Weil das Schalenmodell nur eine Vereinfachung ist, die (wie du ja siehst) nicht ganz zutrifft.
Die Energie eines Orbitals ist nicht nur von der Nummer seiner Schale abhängig, sie ergibt sich aus der Schrödingergleichung. Dabei spielen zum Beispiel Dinge wie Abschirmung durch bereits vorhandene Elektronen, Bahndrehimpuls (also die "Form" des Orbitals) oder komplexere Effekte wie Spin-Bahn-Kopplung eine Rolle. Das wird dann beliebig kompliziert.