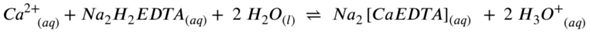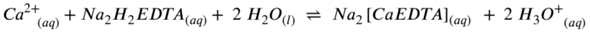Reaktionsgleichungen?
Ich kann diese Aufgabe nicht beantworten.
Formuliere die ausgeglichenen Reaktionsgleichungen für die Reaktion von Na2H2EDTA(aq) mit Ca2+(aq). Begründe, warum das chemische Gleichgewicht jeweils stark auf der Produktseite liegt und warum dies für Titrationen wichtig ist.
2 Antworten

Im Wasser liegt das Ca²⁺ als Hexaaquo-Ion vor; das reagiert mit dem EDTA-Dianion zu einem neutralen löslichen Komplex:
[Ca(H₂O)₆]²⁺ + EDTA²⁻ ⟶ [CaEDTA] + 6 H₂O
Du siehst, daß sich die Teilchenzahl von 2 auf 7 erhöht, das ergibt einen satten Entropiegewinn, der das Gleichgewicht nach rechts treibt (der Komplex ist auch energetisch stabil, und das hilft auch). Da das Gleichgewicht rechts liegt, läuft die Reaktion so gut wie quantitativ ab; deshalb kann man sie für Titrationen verwenden (da will man ja mindestens 99%, besser 99.9% Umsatz).

EDTA ist ein sechszähniger Komplexbildner und bildet besonders stabile 1:1 Chelatkomplexe mit Kationen der Ladungszahl 2+.