Grenzformeln von Naphthalin?
Hey, ich wollte mal fragen wie das bei der Mesomerie von Naphthalin läuft. Kann es sein, dass sich bei einer der 3 Grenzstrukturen, also von dieser:
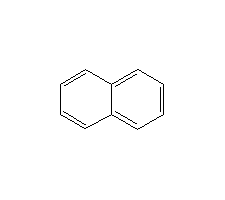
auf diese
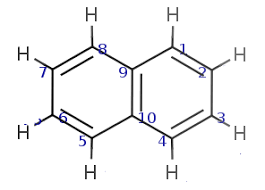
nur die Elektronen von dem rechten Benzenring umklappen?
2 Antworten

Da klappen keine Elektronen um. Man kann mehrere mesomere Grenzformeln für Naphthalin formulieren, dies ist aber dem Umstand geschuldet, dass man mit einer einzigen Skelettstruktur die tatsächlichen Bindungs-Verhältnisse nicht präzise wiedergeben würde.
Naphthalin ist ein Aromat. Hierbei liegen die Kohlenstoffatome sp2-hybridisiert vor. sp2-Hybdridorbitale bilden das Grundgerüst, gleichzeitig überlappen die p-Orbitale und die Elektronen des pi-Systems sind über den gesamten Aromaten delokalisiert.
Dort eingezeichnete "Einfachbindungen" und "Doppelbindungen" sind eigentlich keine, tatsächlich unterscheiden sich die Bindungen nicht. Du hast z. B. auch überall die gleichen Bindungslängen.

Du solltest immer im Hinterkopf behalten, dass dieses Umklappen nur der Veranschaulichung dient. Zweigezackte Pfeile bezeichnen eigentlich Elektronenpaarverschiebungen, wie sie in chemischen Reaktionen auftreten. Wenn man solche Pfeile in mesomeren Grenzformeln sieht, sollte das immer mit einem Augenzwinkern passieren.
Ansonsten kann dir dieses Umklappen helfen, sinnvolle mesomere Grenzformeln zu finden. Wenn man zu Stoffen viele mesomere Grenzformeln formulieren kann, ist das ein Indiz dafür, dass sie besonders stabil sind, da es für das Molekül einen energetischen Vorteil bringt, wenn sich die Elektronen gut über das Molekül verteilen können. Hierbei muss man unbedingt noch beachten, dass diese Grenzformeln sinnvoll sein sollten. Man kann auf dem Papier tausende Grenzformeln zu einem Molekül formulieren, aber das hat dann mitunter nichts mit der Realität zu tun.
Sinnvoll wäre es, so wie in deinem Beispiel, Naphthalin mit 2 Grenzformeln anzugeben. Weniger realistisch wäre es z. B., wenn du es so zeichnest, dass 9 der 10 Pi-Elektronen auf das gleiche Kohlenstoffatom wandern und du dort eine neunfache negative Ladung hättest usw.

Ja schon. Aber das ist halt auch nur eine Zeichnung zum Verständnis der Mesomerie. Im echten Molekül klappt da selbstverständlich gar nichts um.

Erstmal Danke für die Antwort, dass die Elektronen in echt nicht umklappen ist mir bewusst, für unsere Schulaufgabe sollen wir die Grenzstrukturen dennoch darstellen, weshalb ich mir die frage gestellt habe.

Ja das passt schon so. Die untere Grenzformel ist ja auch die "mittlere" aus der man die beiden anderen durch umklappen in den jeweils linken oder rechten Ring erzeugt.

Achso, also ist das im Prinzip der Ausgangspunkt für die Grenzstrukturen

Für die anderen beiden ja. Den zweiten Strich der Doppelbindung zwischen 9 und 10 könntest du ja entweder links oder rechts zeichnen. Das wäre ja dasselbe. Und den klappst du dann in einen der Ringe.
Die beiden anderen Grenzformeln sehen beide so aus wie die obere nur eben jeweils gespiegelt. Sieht man hier ganz gut
Danke nochmal fürs aufklären, die sp2-Hybridisierung und das Naphthalin nicht wirklich so vorliegt sowie der Fakt, dass alle Elektronen delokalisiert sind ist mir bewusst, für eine Schulaufgabe sollen wir dennoch die Grenzformeln mit umklappen der Elektronen darstellen.