Molekülbau; Strukturformel von N20?
Hallo,
ich verstehe delokalisierte Elektronen und die Mesomerie nicht so ganz.
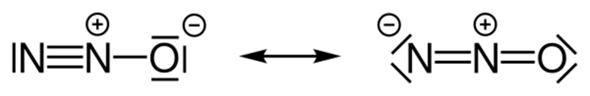
Dies hier sind die zwei Strukturformeln von N2O. Sollte die Regel, dass sowohl bindende als auch nicht-bindende Elektronen Bindungen eingehen können, gelten ist mir diese Abbildung klar. Dann würde jedoch eine Hybridisierung stattfinden, nicht wahr?
Jedoch könnte man dann ja auch auf mehrere Lösungen als nur diese beiden kommen, oder?
Z.B.:

1 Antwort
Jedoch könnte man dann ja auch auf mehrere Lösungen als nur diese beiden kommen, oder?
5 bindiger Stickstoff? Eher nicht.
Eine Hybridisierung findet da übrigens auch nur zum Teil statt. Es gibt zwei sp-Hybridorbitale (die bilden je eine Bindung vom N zum zweiten N und zum O - vom mittleren N aus gesehen). Die anderen Bindungen kommen von unhybridisierten p-Orbitalen (wie bei allen anderen Mehrfachbindungen auch).