Chemie; Orbitalmodell und Atombindungen?
Hallo erstmal,
ich hoffe, dass es hier vielleicht einige Chemie Experten gibt, die mir wegen folgender Situation weiterhelfen können:
Ich nehme im Chemieunterricht gerade Atombindungen durch. Mein Lehrer hat uns diese mithilfe von Orbitalen erklärt, indem er uns sagte, dass die Valenzschale eines Atoms immer halb so viele Orbitale umfassen kann, wie es Elektronen gibt (sprich 4 Orbitale ab der K Schale), dass Orbitale erst einfach besetzt werden, dass sie nie mit mehr als 2 Elektronen besetzt sind und den größtmöglichsten Abstand zu einander haben wollen. Bei einem Orbital ist die Position also egal, bei zweien ist sie linear, bei dreien trigonalplanar und bei vieren tetraedrisch.
Zum Tetraeder hätte ich nun eine Frage. Wir hatten die Aufgabe ein Sauerstoffatom in Lewis-Schreibweise darzustellen. Dabei hat unser Lehrer uns erklärt, dass es absolut falsch sei, wenn die Striche (Elektronenpaare) bei dieser Schreibweise gegenüber liegend wären. Gegen den Uhrzeigersinn gelesen wäre also O Strich, Punkt, Strich, Punkt falsch und O Strich, Strich, Punkt, Punkt richtig. Ich verstehe nicht weshalb, mein Lehrer meinte, dass es am Tetraederwinkel liege, der unter dieser Vorraussetzung zwischen den einzelnen Elektronen nicht vorhanden wäre, wodurch es kein Tetraeder mehr wäre.
Aber weshalb? Beim Kohlenstoff zum Beispiel sind alle Orbitale einfach besetzt und werden zu jeder Seite in der Lewis Schreibweise um das C herum geschrieben. Dort ist es doch auch ein Tetraeder. Die Tatsache, dass es ein vollbesetztes Orbital an der Stelle eines einfach besetzten ist, ändert doch nichts an der räumlichen Form des Tetraeders(?). Warum also darf ich die Position der 2 Striche um das O beim Sauerstoff nicht beliebig festlegen, solange es wie beim C-Atom einem + um das O oder einem Kreuz (so bevorzugt es mein Lehrer) entspricht?
Ich hoffe wirklich meine Frage ist halbwegs verständlich und jemand hier kann es mir erklären:)
Danke!
1 Antwort
Also wenn ich das richtig verstanden habe, dann meinst du, warum man das Wassermolekül so zeichnet

und nicht so H-O-H (mit den Elektronenpaaren unter und über dem O)
Richtig?
Das ist ein Problem Art der Zeichnung und nicht der Orbitalbesetzung. Eine Zeichnung der Art H-O-H impliziert immer ein lineares Molekül. Wasser ist aber nicht linear.
Daher wird es, um den tetraedrischen Bau deutlich zu machen, so gezeichnet wie oben im Bild.
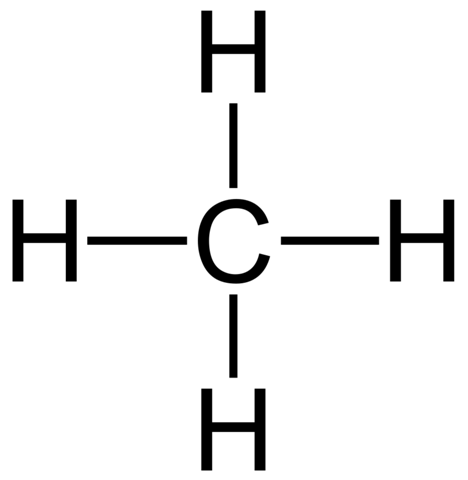
Um das nochmal etwas zu verdeutlichen. Methan kann man so zeichnen:
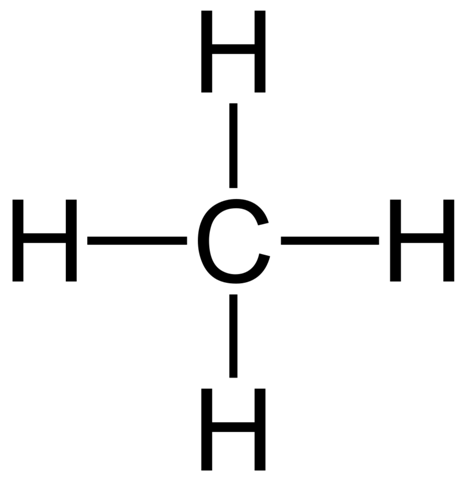
Das ist aber genau genommen auch falsch, weil die Zeichnung aussieht als wäre das Molekül planar. Dem ist aber nicht so. Richtigerweise müsste man es also so zeichnen:
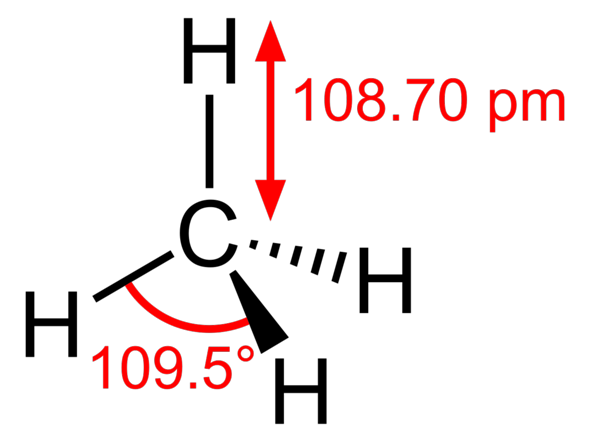
Macht aber kaum jemand, weils zu umständlich ist.

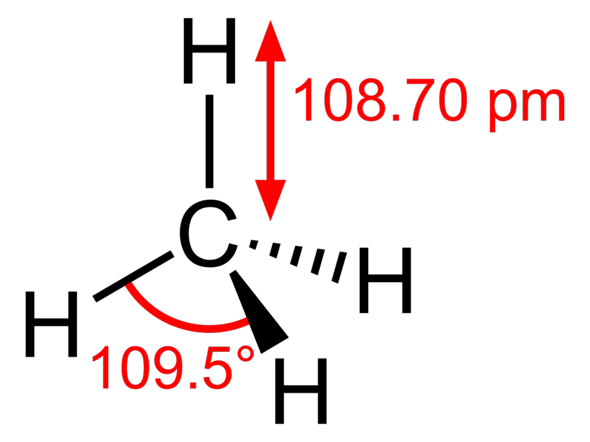
*ich meinte gegenüber und nicht nebeneinander in der 4. Zeile
Ach so, du meinst bei einem einzelnen Sauerstoffatom ohne Bindungen? Da ist die Diskussion sinnfrei, weil es keinen Tetraeder gibt. Ein Tetraeder würde hybridisierte Orbitale voraussetzen, die hast du bei einem einzelnen Atom aber nicht. Ergo ist es egal, wo du die gepaarten bzw ungepaarten Elektronen hinzeichnest.
Es sitzen 2 im s-Orbital, 2 in einem der p-Orbitale und je eines in den anderen beiden p-Orbitalen. Das kann man aber zeichnerisch kaum darstellen. Visualisiert schaut das ungefähr so aus https://en.wikipedia.org/wiki/Atomic_orbital#/media/File:Schrodinger_model_of_the_atom.svg
Genau das meinte ich; ich frage mich nur, was mein Lehrer dann mit seinem Tetraeder meint. Laut ihm wäre es nämlich so, dass beim Lithiumatom ein Orbital gebildet wird, bei Beryllium zwei Orbitale, die sich quasi gegenüberstehen, bei Bor 3, in der Form eines Dreiecks (ungefähr) und bei Kohlenstoff 4, die einen Tetraeder bilden. Der Aufbau wäre also so ähnlich wie bei dem Methan in Keilstrichformel, was du geschickt hast, nur dass das C in dem Falle der positive Kern wäre und die Orbitale sich an den Stellen befinden, wo H steht. So wäre es dann auch beim Sauerstoff und deswegen meint er, dass es eben nicht egal sei, wo die gepaarten und wo die ungepaarten Elektronen hingezeichnet werden. Hast du vielleicht eine Ahnung, wie er das meinen könnte, wenn es eigentlich ja gar keinen Tetraeder geben kann?
Zuerst mal werden keine Orbitale "gebildet". Die sind immer da, in Form von Energieniveaus, ums mal so zu umschreiben. Auch z.b. ein Sauerstoffatom hat d-Orbitale. Die sind energetisch aber so weit weg, dass sie nicht besetzt werden.
Woher er das hat weiß ich auch nicht. Hybridorbitale gibt es nur bei Bindungen, nicht bei einzelnen, ungebundenem Atomen. Ein Atom hat keinen Grund Hybridorbitale zu bilden, wenn es keinen Bindungspartner hat.
Kannst ihn ja mal fragen, wie er dann die sp und sp2 Hybridisierung beim Kohlenstoff erklärt, wenn es doch angeblich im ungebundenen Zustand sp3 hybridisiert bzw tetraedrisch sein soll.
Hallo, vielen Dank erstmal! Bei einer Verbindung habe ich das jetzt so weit verstanden, aber weshalb ist es bei einem einzelnen Sauerstoffatom, welches sich in keiner Verbindung befindet so, dass die Elektronenpaare (besetzte Orbitale) in der Lewis-Schreibweise nicht nebeneinander sein dürfen. Also angenommen ich nehme jetzt den Sauerstoff und zeichne ihn so, wie du das Wassermolekül gezeichnet hast (nur eben ohne H) und an den Stellen wo eigentlich das Elektronenpaar zwischen O und H wäre mache ich die Punkte für die einzelnen Elektronen (halb besetztes Orbital). Das wäre nun richtig laut meinem Lehrer. Würde ich nun aber den rechten Punkt und den rechten Strich tauschen, so wäre es falsch, weil laut meinem Lehrer kein Tetraederwinkel mehr vorhanden wäre. Das verstehe ich nicht.