Äquivalenzpunkt anhand einer Titrationskurve bestimmen?
Hallo,
ich habe diese Aufgabe zur Titration
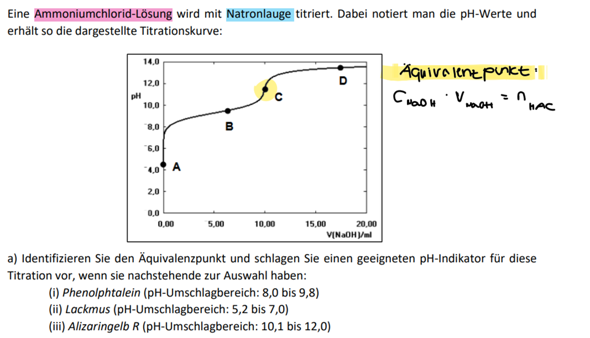
Ich verstehe hier nicht wie man auf den Äquivalenzpunkt kommt. Weil den Äquivalenzpunkt berechnet man ja cxV=n.
Zum Beispiel wäre der Äquivalenzpunkt bei folgenden Beispiel: "10ml Essigsäure mit der Konzentration 0,1 mol/l werden mit 0,1 mol/l Natronlauge titriert"
--> cxV= 0,1 mol/l x 10ml = 1, d.h ÄP= 1 oder?
Aber wie lese ich den Äquivalenzpunkt an der Titrationskurve ab? :)
2 Antworten
Weil den Äquivalenzpunkt berechnet man ja cxV=n.
Nein. mit n = c * V berechnet man die Stoffmenge.
Am Äquivalenzpunkt gilt dann (bei Säure-Base-Titration)
n(Säure) = n(Base)
--> cxV= 0,1 mol/l x 10ml = 1,
Schon dashalb falsch, weil die Einheit fehlt.
d.h ÄP= 1 oder?
1 Mol? Keinesfalls.
Außerdem geht es hier um einen Punkt, und der wird, wie aus dem Matheunterricht bekannt, durch zwei Koordinaten (in der Ebene) bestimmt.
Üblicherweise sagt man eher "Der ÄP liegt bei pH = ..." (und die zugehörige Stoffmenge entnimmt man aus dem Diagramm) oder "Der ÄP wurde nach V = ... erreicht" (und mittels c ergibt sich daraus dann die Stoffmenge).
Aber wie lese ich den Äquivalenzpunkt an der Titrationskurve ab? :)
Es ist der Punkt mit der größten Steigung, der obendrein in der Nähe des erwarteten pH-Wertes liegt.
es ist der größte Punkt,
Nein. Ich schrieb - etwas unsauber - von dem Punkt, an dem die Titrationskurve die größte Steigung hat (solltet Ihr Steigung in Mathe noch nicht kennen: da, wo die Kurve am steilsten ist)
der obendrein in der Nähe des erwarteten pH-Wertes liegt
Eventuell ist bei A die Steigung noch größer. Aber das ist trotzdem nicht der ÄP, weil der pH-Wert im Sauren liegt, während bei dieser Titration (schwache Säure mit starker Base) der ÄP im alkalischen liegen muss. Obendrein kennt man ja ganz grob die zu erwartende Menge an NaOH, auch deshalb scheidet Punkt A aus.
Das ist der Punkt C. Dort ist ein pH-Sprung. Nun kannst du aus dem Diagramm das Volumen der NaOH ablesen und in deine Formel einsetzen.
Voll gut erklärt! Danke ;) Aber was meinst du mit "es ist der größte Punkt, der obendrein in der Nähe des erwarteten pH-Wertes liegt"? :)