Hi, kann mir jemand bei der folgenden Aufgabe helfen?
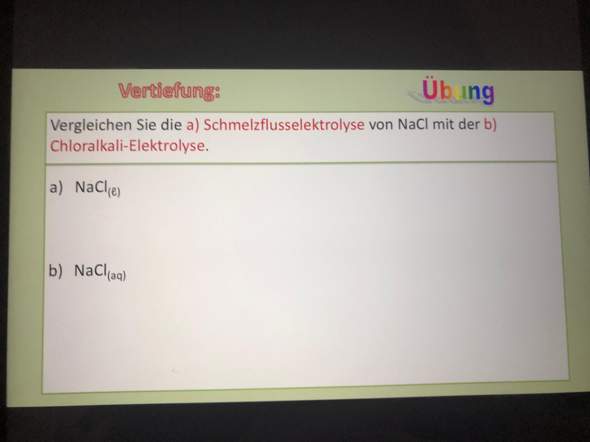
Begründen Sie, warum wässrige Lösungen der Salze Natriumhydrogencarbonat und Natriumhydrogenphosphat alkalisch reagieren.
Mein Ansatz:
Bei Natriumhydrogencarbonat erfolgt die Reaktion durch die Bildung von Hydroxidionen (OH-) aus dem Wasser und der Carbonation (HCO3-) aus dem Salz. Bei Natriumhydrogenphosphat entstehen ebenfalls Hydroxidionen. Diese Hydroxidionen machen die Lösung alkalisch.
Die Konzentration der OH-Ionen überwiegt der Konzentration an Hydroniumionen (H3O+), weshalb die Lösung alkalisch reagiert.
Stimmt das so? was kann ich verbessern?