welche Verbindung ist das in Chemie?
hallo, ich weiß hier leider nicht, um welche Verbindung es sich handelt, es wäre mega nett, wenn mir das jemand sagen kann :)
also über S und O steht halt die Wertigkeit und darunter halt eingekreist das kgV :)
mia :)

meine Verbindung lautete: Schwefel(VIII)-oxid
2 Antworten

Ein Schwefel(VIII)-Oxid gibt es nicht.
Was du dort vorliegen hast ist das Sulfat-Ion, bei der Schwefel nicht die OZ +8, sondern +6 trägt, somit das Sulfation 2-fach negativ geladen ist.
Das Sulfation ist das Säurerestion der Schwefelsäure (H₂SO₄):
SO₄²-
Es gibt eine sehr exotische neutrale SO₄ Verbindung, das Schwefeltetroxid. Allerdings trägt auch in dieser Verbindung Schwefel die OZ +6. Diese ist jedoch so exotisch, dass es nicht mal einen Wikipedia-Eintrag dazu gibt.



Klaro https://en.m.wikipedia.org/wiki/Higher_sulfur_oxides
Viele Worte werden da aber nicht verloren.

Vielen Dank! Habe auf die Schnelle nichts gefunden. Das sind in der Tat wenige Worte.
Im Holleman/Wiberg wird es auch nur in einer Tabelle aufgeführt, aber mehr auch nicht.

Liegt denk ich mal daran, dass es instabil und chemisch relativ uninteressant ist

Ich muss auch ehrlicherweise sagen, dass ich es bis zu der Frage auch nicht auf dem Schirm hatte…

So gings mir auch. Aber es gibt immer ein paar so Knaller, die alle möglichen abstrusen Verbindungen machen xD

Ohja… das abstruseste was ich bis jetzt gesehen habe war NaCl₃.

Das ist auch nicht schlecht xD
In der letzten Anorganik Vorlesung kamen auch Dinger vor. Zum Beispiel ein metallisch leitendes (SN)x Polymer. Und Bor hat sowieso allerhand abgefahrene Verbindungen geliefert

meine Verbindung lautete: Schwefel(VIII)-oxid
Das bezweifle ich aber ganz ganz stark. Ein Schwefelatom in der Oxidationsstufe +8 existiert nämlich nicht (kann es auch gar nicht). Das höchste der Gefühle für Schwefel ist +6.
Sollte das tatsächlich ein SO4 sein, dann handelt es sich um Schwefeltetroxid. Das kann aber nur bei sehr tiefen Temperaturen erzeugt werden (weil instabil) und sieht so aus:
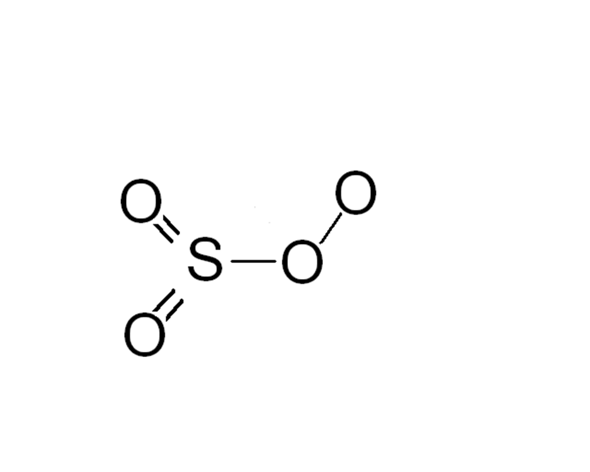
Wie du siehst, hat auch hier der Schwefel eine Oxidationsstufe von +6, da das ein Peroxid ist.
Wahrscheinlicher ist allerdings dass es sich bei deiner Verbindung um das Sulfation handelt, also SO4^2-. Das ist stabil und auch da hat der Schwefel eine Oxidationsstufe von +6.
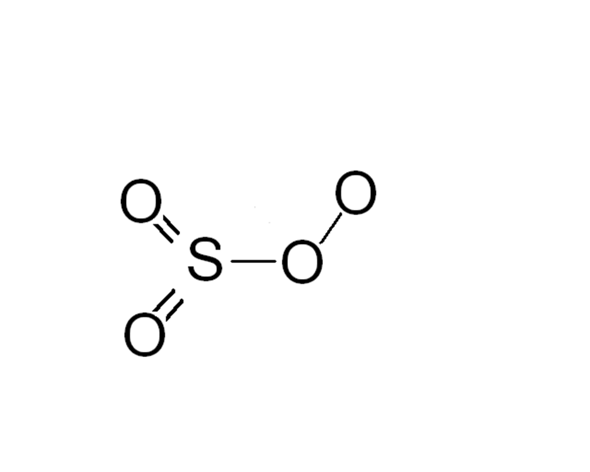

Den Eintrag gibt es tatsächlich, allerdings in der englischen Wikipedia ;)