Was kommt am Ende raus als edelgaskonfiguration?
Ionische Bindung Gallium gibt seine außenelektronen ab und Sauerstoff bekommt sie aber was steht da am Ende? 6- und 6+??
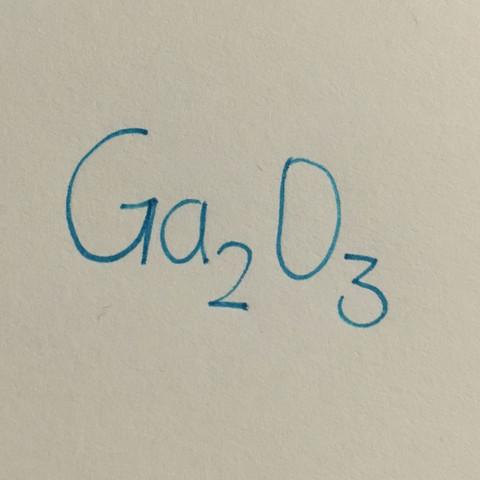
6 Antworten
wo soll das stehen?
Nicht alles strebt eine Edelgaskonfiguration an, noch weniger erreicht diese auch.
Beim Sauerstoff besteht da kein Problem, jedes O-Atom nimmt 2 Elektronen auf, wird zum Oxid-Ion und hat damit die Elektronenkonfiguration des Neon.
Ga müsste schon 13 Elektronen abgeben, um die Elektronenkonfiguration des Ar zu erreichen, was völlig unmöglich ist.
Oder 5 aufnehmen, zu Elektronenkonfiguration des Kr. Ist auch unmöglich, da Ga ein Metall ist und lieber Elektronen abgibt.
Es gibt für Metalle allerdings auch eine andere stabile Konfiguration, die kaum/nicht weniger stabil ist.
Bin aber im Zweifel, ob du das überhaupt verstehen kannst, wovon ich rede.
Das Ion Zn²⁺ ist das bekannteste Beispiel.
Da ist die äußerste Schale geleert worden, und die zweitäußerste "befriedigt".
[Für die Experten, die d-Orbitale der zweitäußersten Schale sind komplett voll, und inzwischen energetisch deutlich niedriger als die s-Orbitale der äußersten.]
Für dich gilt jedenfalls, dass Ga 3 Elektronen abgibt, zum Ion Ga³⁺, und damit einen ziemlich stabilen Zustand erreicht, auch wenn der nicht Edelgaszustand genannt wird.
[Für die Experten, wenn die Bindung als nicht rein ionisch betrachtet wird, teilt sich das Ga-"Ion" vier bindende E.-Paare mit dem Sauerstoff, und erreicht so doch irgendwie die Konfiguration des Kr. Dagegen spricht jedoch die oktaedrische Koordination. Oder vielleicht auch nicht, wenn π-Bindungen beteiligt sind.].
Am Ende steht jedenfalls Ratlosigkeit. Für mich.
Für dich gibt jedes Ga 3 Elektronen ab, und jedes O nimmt 2 auf, nicht anders als beim Aluminiumoxid.
Nur erreicht Al dadurch eine Edelgaskonfiguration, Ga eine andere, (fast) genau so stabile. Die hat nur keinen Namen, oder ich kenne ihn nicht.
Das mit dem 9 stimmt deswegen verstehe ich das auch nicht wenn es 8 wären wäre es Neon oder ?
Gallium hat 3 Aussenelektronen und Sauerstoff 6.
Wenn Gallium 3 abgibt, hat Sauerstoff 9 und wäre damit keine Edelgaskonfiguration (Volle Aussenschale)
Nein, du kannst nicht einfach irgendwelche Zahlen miteinander verrechnen wie du willst.
3 Sauerstoffatome haben jeweils 2 Elektronen aufgenommen und besitzen demnach 8 Elektronen auf der äußeren Schale, haben also Edelgaskonfiguration.
2 Galliumatome haben jeweils 3 Elektronen abgegeben, haben also 8 Elektronen auf der äußeren Schale, also auch Edelgaskonfiguration.
In dieser Verbindung hast du Ga(3+) Ionen und O(2-) Ionen. Was ist genau die Frage?
Aber Gallium hat jeweils 3 und Sauerstoff Hat jeweils 6 ( und die Aufgabe ist ja Ga2 und O3 also kann man ja quasi 3*6=18 rechnen und es braucht aber 24 um alle 3 voll mit 8 außenelektronen zu füllen und 2*3=6 also passt es ja oder nicht ?