Partialladung - Trichlormethan?
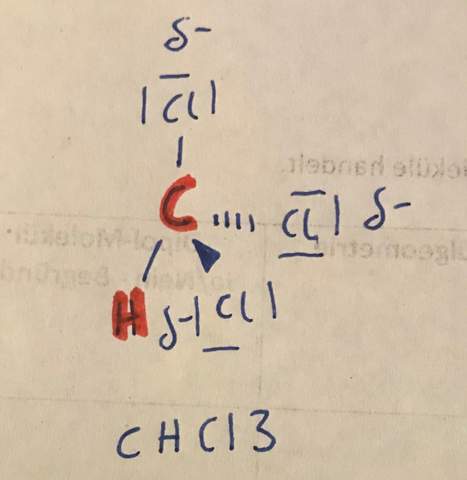
Also Cl muss ja eine negative Partialladung besitzen, aber wie bestimmt man die Partialladung von C und H? Vergleicht man dann alle drei oder wie?
Danke :)
3 Antworten
Also wenn man C und Cl vergleicht, bekommt das Cl die negative PL und entsprechend das C die positive PL. Das hast du soweit schon richtig erkannt.
Wenn man C und H vergleicht, bekommt H die positive PL und C die negative PL.
Da entsteht jetzt ein Konflikt: Bekommt das C nun eine positive oder eine negative PL?
Lösungsvorschlag 1: Wenn positiv und negativ im Konflikt stehen, lass es einfach neutral. Das hebt sich in etwa auf.
Lösungsvorschlag 2: Die drei negativen Chloratome "gewinnen" gegen das eine positive H-Atom. Deswegen ist das C eher positiv als negativ.
Lösungsvorschlag 3: Am besten wäre, wenn du dir zur Darstellung der Ladungswolke ein 3D-Modell bastelst und darin die Ladungswolke mit Watte einklebst. Das kommt der Realität am nächsten.
Hilft dir das weiter?
Ich habe für Dich mal in die Trickkiste der physikalischen Chemie gegriffen (naja mit Hilfe meines Programmes).
Schauen wir uns mal die berechneten Ladungen am Trichlormethan an
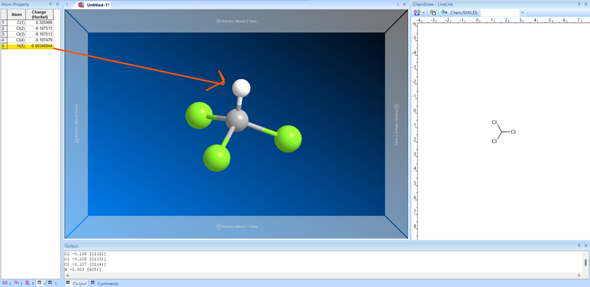
Wir korrekt vorhergesagt, haben die drei Chloratome (da gleichwertig), etwa die selbe partielle negative Ladung, die sie dem Kohlenstoffatom entziehen und zwar ziemlich genau ein drittel der Ladung die dem Kohlenstoff fehlt. Nun vergleichen wir die EN Werte von Kohlen- und Wasserstoff und stellen fest, dass Wasserstoff etwas schlechter ist. Das bedeutet, dass das Elektronentauziehen vom Kohlenstoff gewonnen wird bzw. nur sehr knapp gewonnen wird.
Zum Vergleich: Beim Methan hat das Wasserstoff eine Ladung von 0,05 hier -0,003. Das ist zwar eine Veränderung, die aber keine große Rolle spielt.
Hätte das Wasserstoffatom eine deutlich stärkere positive Ladung wäre es azide, das ist aber gerade nicht der Fall. TCM ist weit davon entfernt auch nur irgendwie eine Säure unter normalen Umständen zu sein.
Ebenfalls ist TCM alles andere als polar (schwer wasserlöslich). Hoffe das hilft Dir weiter
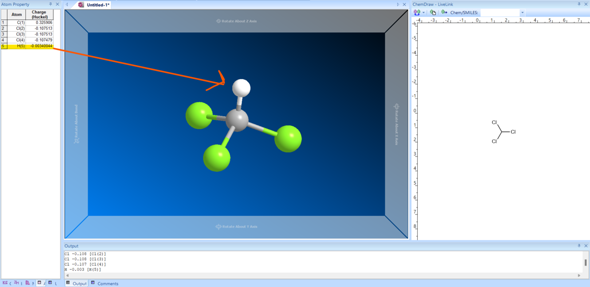
Da sich die Elektronegativitäten von C und H nicht groß unterscheiden, fällt auch das Ausmaß der Ladungsverschiebung zwischen den beiden relativ gering aus.
Hier gibt es eine Formel, mit der man das abschätzen kann: https://de.m.wikipedia.org/wiki/Partialladung
Ich nehme an, dass das der Grund ist, warum Partialladungen bei C-H-Bindungen oft ignoriert werden.
Normalerweise wird bei der Bestimmung von Partialladungen nur die fragliche Bindung angeschaut und die nächste Umgebung ignoriert.
In diesem Fall, kann man aber wohl argumentieren, dass das C durch die Einflüsse der drei Cl schon sehr stark partiell positiv geladen ist. Daher ist davon auszugehen, dass es die Elektronen der C-H-Bindung stärker zu sich zieht, als es z.b. in CH4 der Fall wäre. Insgesamt wird aber wohl trotzdem eine partiell positive Ladung am C zurückbleiben, da der Einfluss der Cl deutlich überwiegt.