Säurestärke/Basizität anhand Strukturformeln ermitteln?
Kann mir jemand erklären, wie man die Säurestärke/Basizität anhand der Strukturformeln erkennen und im Vergleich zu anderen reihen kann? Die Aufgabe sieht wie folgt aus. Am liebsten wär mir ein Schema F, das ich immer wieder anwenden kann. DANKE!
1 Antwort
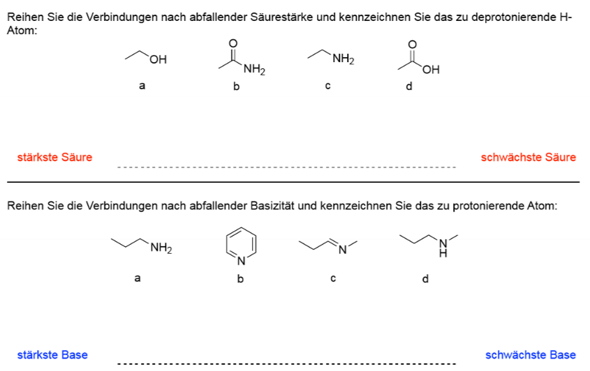
Dass die Essigsäure mit pKa = 4,75 die Reihe anführt, ist wohl selbstredend. Und auch die letzte Position ist leicht zu ermitteln. Das Ethylamin ist die Verbindung, die am basischsten ist und somit zwangsläufig die schwächste Säure. Beim Acetamid ist die Basizität des Stickstoffs durch Mesomerie mit der C=O-Doppelbindung deutlich reduziert, was sich in einer gegenüber Aminstickstoff erhöhten Acidität äußert. Dabei könnte ich ohne Recherche nicht beurteilen, ob Acetamid oder Ethanol saurer ist. Ich weiß nur, dass beide nur sehr starken Basen ihr Proton überlassen. Nach Recherche findet man für Ethanol einen pKa von 15,9 und für Acetamid von 15,1.
Sekundäre Amine sind stärker basisch als primäre und diese basischer als Ammoniak (+I-Effekt der Alkylgruppen) daher kommt das Methylpropylamin auf Position 1. Die Imine sind weniger basisch als die entsprechenden Amine. Ich würde daher das Propylamin auf Position 2 setzen und das Imin auf 3. Das Pyridin ist sicher die schwächste Base.