Ist Ethanol (C2H6O) polar oder unpolar?
Hi,
ich würde gerne wissen, ob Ethanol polar oder unpolar ist und eine allgemeine Regel dafür erfahren. Zur Bestimmung wird ja eigentlich nur die Differenz Elektronegativitäten genommen, aber ich habe ja hier mehrere Dinge miteinander "agieren".
Ich bin schon so weit:
∆EN(C-C): 0
∆EN(C-0): 0,8
∆EN(O-H): 1,2
Laut dem ersten müsste Ethanol ja unpolar sein, nach den anderen beiden aber polar. Wie genau ist das nun? Wird Ethanol jetzt als polar oder unpolar gesehen?
Vielen Dank für jede Hilfe im Voraus,
Till
2 Antworten
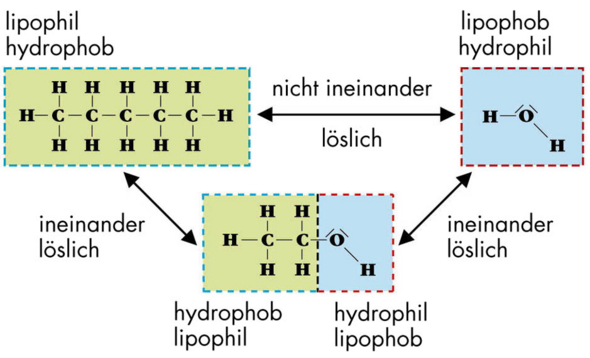
Ethanol besteht aus einem unpolaren Teil, dem Alkylrest und einem polaren Teil, der Hydroxygruppe.
Die polare Hydroxygruppe ist dafür verantwortlich, dass Wasserstoffbrücken ausgebildet werden können, weswegen Ethanol wasserlöslich ist.
Des Weiteren sorgt der unpolare Alkylrest dafür, dass das Ethanolmolekül mit unpolaren Stoffen wie beispielsweise Benzin wechselwirkt, was auf die Van-der-Waals-Wechselwirkungen zurückzuführen ist, weswegen Ethanol auch fettlöslich ist.

(Quelle: http://www.seilnacht.com/Chemie/ch_ethol.htm)
Das heißt, dass unser Ethanol wasserlöslich ist und sich auch in Stoffen wie Pentan oder anderen Alkanen löst.

(Quelle: https://www.chemie.schule/j11/j11lh/basiswissen_alkanole.htm)
Das heißt, dass Ethanol auch als Lösungsmittel geeignet ist.
~Johannes
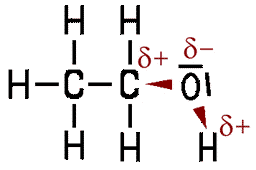
Ethanol hat nur einen teil der Polar ist. Also nur die OH Gruppe vom Ethanol ist Polar der Rest nicht
Eben wegen der OH Gruppe Löst sich das Ethanol im Wasser und eine Wasserstoffbrückenbindung liegt meine ich auch vor.
Da das Molekül auch sehr klein ist, ist der Einfluss der OH Gruppe auch sehr stark deswegen ist zB Ethanol auch unbegrenzt Wasserlöslich.
Und wie ist das jetzt mit der Löslichkeit in Wasser? Wir haben gelernt, dass gleiches sich in gleichem löst, aber wie ist das wenn ein Teil gleich und der andere Teil ungleich ist?