Farbveränderung durch Wasser?
Gegeben ist: 84 g blaues Kupfer(Il)-sulfat-Pentahydrat werden ent-wässert. Dabei entstehen 53,7 g weißes wasserfreies
Kupfer(Il)-sulfat.
daraus soll man den prozentualen Masse Anteil Wasser im Kupfer(Il)-sulfat-Pentahydrat berechnen
1 Antwort
Vom Beitragsersteller als hilfreich ausgezeichnet
Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer
Wasser, Reaktion, chemische Reaktion
Nun, offensichtlich stecken 84−53.7=30.3 g Wasser in der Probe, das sind w=30.3/84=36.1%.
Mit diesem Meßergebnis kann man aus den molaren Massen auch ausrechnen, wieviel Moleküle Kistallwasser im Kupfersulfat drinstecken. Wenn wir die unbekannte Zahl an Kristallgewässern x nennen, dann bekommen wir:
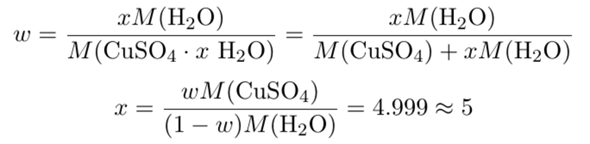
Kristallwasserhaltiges Kupfersulfat ist also ein Pentahydrat.
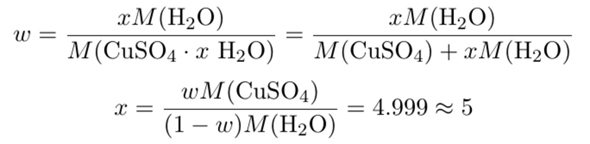
Danke das sie mir geholfen haben die Aufgabe habe ich jetzt verstanden könnten sie mir noch weiter helfen?