Chemie Darstellung Hydrathülle /Hydratisierte Ionen?
Hi wir müssen in Chemie Hydratisierte Ionen von Säuren die mit Wasser vermischt werden darstellen.
Allerdings habe ich echt keinen Plan davon.
Könnte mir jemand die Vorgehensweise erläutern !?
2 Antworten

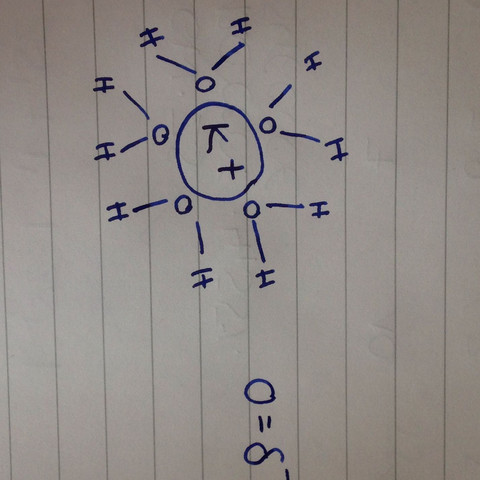
Der Sauerstoff im Wassermolekül ist negativ partiell geladen. Das liegt am permanenten Dipolmoment des Moleküls.
Positiv und negativ zieht sich an, deshalb ist ein Kation (+) von den Sauerstoffmolekülen des Wassers umgeben.
LG

Du sprichst von Säureionen. Da verstehe ich nicht ganz, wieso du Kalium als Kation hast. Habt ihr Säuren vorgegeben, die ihr darstellen sollt?
Da ihr wahrscheinlich nur Säuren nach Bronstedt behandelt habt, wären das zb HCl, H2SO4...
Da wäre das Kation, dein Wasserstoffion, welches nicht Hydratisiert ist sondern mit Wasser ein H3O^+ Ion bildet. Also sollt ihr wahrscheinlich eher Anionen (Cl^-, SO4^2-...) darstellen, oder?

Da steht aber nichts davon eine Hydrathülle darzustellen sondern nur die Ionen zu nennen. zB dissoziiert (so schimpft sich die Reaktion wenn man Säure oder Base in Wasser gibt) Salzsäure zu H+ und Cl- (streng genommen: HCl + H2O ---> Cl- + H3O+)
Nenne doch mal alle Säuren/Basen die du in der AUfgabe gegeben hast und schreib dahinter mal die Ionen, wie du meinst dass sie richtig sind. Dann können wir sehen was du verstehst oder nicht verstehst und dir besser helfen :)

Oha jetzt kommts
Blausäure HCN+H2O -> H3O+CN
Schwefelsäure N2SO4+H2O -> H2O5 N2 S1
Salpetersäure HNO3 +H2O -> H3O N1
Iodwasserstoffsäure HI +H2O ->H3O I1
Lithiumhydroxid LiOH +H20-> H3O2 Li
Vielleicht so

ich Nummeriere das mal durch, wegen der Übersichtlichkeit.
1. Ladungen fehlen (Ionen sind positiv oder negativ geladen, wichtig!)
2. Schwefelsäure ist nicht N2SO4, Ladungen fehlen, und die Produktseite ist auch echt schief glaufen :P (das Ionen der Schwefelsäure ist HSO4-, bzw SO42-)
3. Ladungen fehlen, auf der linken Seite müssen immer genau so viele Atome wie auf der rechten sein, das Ion ist falsch N1 gibt es nicht und wäre hier auch fehl am Platz.
4. Ladungen fehlen, wenn es nur ein Atom ist schreibt man 1 nicht in den Index (tieferstellen), ansonsten garnicht schlecht.
5. LiOH ist eine Base, Basen werden in Wasser zu einem Metalkation und einem Hydroxidanion (OH-)
Also, wichtig sind die Ladungen, und dass du mal im Buch anschaust was eine Säure/Base auszeichnet und unterscheidet. Lies dir dazu auch was zur Dissoziation durch und versuch es nochmal =), aber so schlecht sieht das ja garnicht aus =)

Naja so schlecht sieht das ja gar nicht aus ist noch nett ausgedrückt. Bei solchen Aufgaben sehen ich immer wieder warum ich Chemie im nächsten Schuljahr abgewählt habe

Ach das ist garnicht so wild wie es sich darstellt. Ich habe mich in der Schulzeit genauso wie du gefühlt. Irgendwann fällt einfach der Groschen und alles macht plötzlich Sinn. Und wenn das passiert öffnet sich ein sehr spannendes naturwissenschaftliches Gebiet und du nimmst deine Umwelt plötzlich ganz anders wahr. Schade, dass du Chemie abwählst, aber du weißt, was das beste für dich ist =)
Ich hoffe ich konnte dir trotzdem ein wenig helfen, wenn nicht stell gerne weitere Fragen =)
Ich weiß es nicht. So lautet die Aufgabe : Notiere die Ionen, die entstehen, wenn die folgenden Säuren bzw Basen mit Wasser vermischt werden !
Blausäure HCN
.
.
.