Wirkungsweise von coenzyme?
Hallo, könnte jemand die Abbildung beschreiben und erklären?
1 Antwort
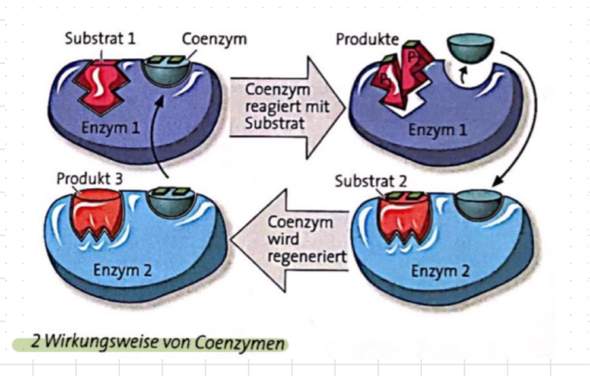
Coenzyme sind notwendig, damit ein Enzym katalytisch aktiv werden kann. Es nimmt in der Regel chemische Gruppen, Elektronen oder Protonen vom Substrat auf oder gibt diese ans Substrat ab. Man kann dabei unterscheiden zwischen prosthetischen Gruppen (das Coenzym ist fest ans Enzym gebunden) und Cosubstraten (das Coenzym ist nicht kovalent ans Enzym gebunden). Im Unterschied zum Enzym wird ein Coenzym während der chemischen Reaktion verändert. Damit es wieder in seiner ursprünglichen Form für weitere Reaktionen zur Verfügung steht, muss es regeneriert werden. Eine solche Wirkungsweise ist in der Abbildung dargestellt.
Versuchen wir mal, das ganze an einem konkreten Beispiel zu verstehen: in der Glykolyse wird schrittweise Traubenzucker (Glucose) zu Pyruvat abgebaut. Die frei werdende Energie wird zur Bildung von ATP, der universellen Energiespeicherform in allen Lebewesen, genutzt. Eine der Zwischenreaktionen der Glykolyse katalysiert das Enzym Glycerinaldehyd-3-phosphat-Dehydrogenase (GAPDH). Es katalysiert die Reaktion des Substrats Glycerinaldehyd-3-phosphat (GAP) zu 1.3-Bisphosphoglycerat (1.3-BPG). GAP wird dabei oxidiert, d. h. es werden zwei Elektronen (und ein Wasserstoff) entfernt. Die Elektronen müssen aber irgendwo hin, deshalb werden sie (zusammen mit dem Wasserstoff) auf das Cosubstrat NAD+ übertragen. NAD+ wird dabei zu NADH reduziert.
In der aeroben Glykolyse schließt sich an die Bildung von Pyruvat der Citratzyklus an, in dem weitere Reduktionsäquivalente (NADH und FADH2) produziert werden. Die werden in der sich anschließenden Atmungskette wieder oxidiert zu NAD+ und FAD, indem die Elektronen schrittweise auf Sauerstoff übertragen werden, der dabei zu Wasser reduziert wird. Die abgegebenen Protonen werden zum Aufbau eines elektrochemischen Gradienten genutzt, der die ATPase antreibt. Die aerobe Glykolyse liefert deshalb viel Energie, setzt aber voraus, dass Sauerstoff vorhanden ist.
Bei der anaeroben Glykolyse, wie sie z. B. viele Bakterien oder Hefen betreiben, ist mit der Bildung von Pyruvat Schluss. Das heißt, dass irgendwann sämtliches NAD+ verbraucht wäre und die Glykolyse zum Stillstand käme. Das in der Glykolyse anfallende NADH muss deshalb in vom Sauerstoff unabhängigen Gärungsreaktionen regeneriert, also wieder in die oxidierte Form NAD überführt werden. Ein Weg ist z. B. die alkoholische Gärung. Das Pyruvat wird dabei erst zu Acetaldehyd umgewandelt (decarboxyliert), es wird CO2 frei. Anschließend reduziert das Enzym Alkoholdehydrogenase (ADH) zu Alkohol (Ethanol), indem sie die Elektronen vom NADH auf das Substrat überträgt. Aus NADH wird wieder die oxidierte Form NAD+. Dieses steht dann wieder für die Glykolyse zur Verfügung.