Wie können Zink- Ionen, die zweifach positiv geladen sind, in der Elektrolyse zur Kathode wandern und da 2 Elektronen aufnehmen?
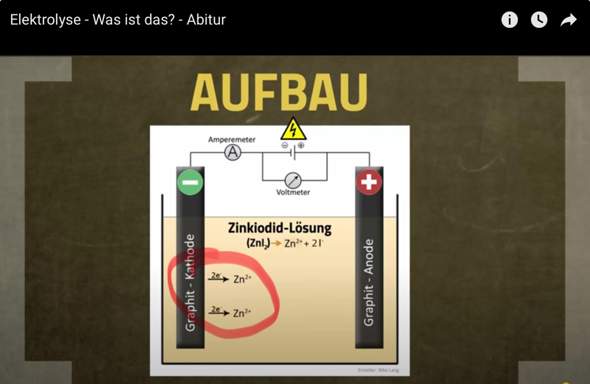
Hallo, ich brauche dringend Hilfe in Chemie zum Thema: „Elektrolyse“. Meine Frage hab ich schon oben geschrieben, aber ich erklär das nochmal genauer. In einem YouTube Video (siehe der Link unten und der Screenshot) wurde erklärt, dass sich in der Zinksulfatlösung, zweifach positive Zink-Ionen und negative Iodid-Ionen befinden. Die Zink-Ionen wandern zur Kathode (Minuspol), da sich ja unterschiedliche Ladungen anziehen. Weiter wird erklärt, dass die Zink-Ionen 2 Elektronen aufnehmen, aber wie können zweifach positive Zink-Ionen Elektronen aufnehmen wenn Zn2+ doch bedeutet, dass Zink 2 Elektronen abgeben muss? Dasselbe mit den negativ geladenen Iodid-Ionen, welche zur Anode (Pluspol) wandern. Diese geben 1 Elektron ab, doch wie geht das, wenn Iod in der 7.HG ist und somit 1 Elektron aufnehmen müsste? Genau das verwirrt mich und ich hoffe dass mir jemand eine Antwort darauf geben könnte. Das würde mir wirklich weiterhelfen! Dankeschön schonmal im Voraus!
Der Link zum Youtube Video: https://youtu.be/EzBAGN2Jx7Y?feature=shared
1 Antwort

Du hast schon recht, dass das eigentlich das passieren müsste. Nur handelt es sich hier um eine Elektrolyse. Die ist genau das Gegenteil von einem normalen galvanischen Element.
In galvanischen Element aus Zn und I würde das hier passieren:
2 Zn + I2 -> Zn^2+ + 2 I^-
Dabei wird Strom erzeugt durch die Elektronenwanderung von der Zink- zur Iod-Halbzelle.
So, bei einer Elektrolyse legst du da jetzt Strom an und zwar in die andere Richtung. Dadurch zwingst du die Reaktion anders herum zu laufen, weil du den Elektronenfluss umgedreht hast. Daher läuft die obige Reaktion jetzt rückwärts:
Zn^2+ + 2 I^- -> 2 Zn + I2