Warum kann Flour nicht elektrochemisch hergestellt werden, aber Chlor schon?
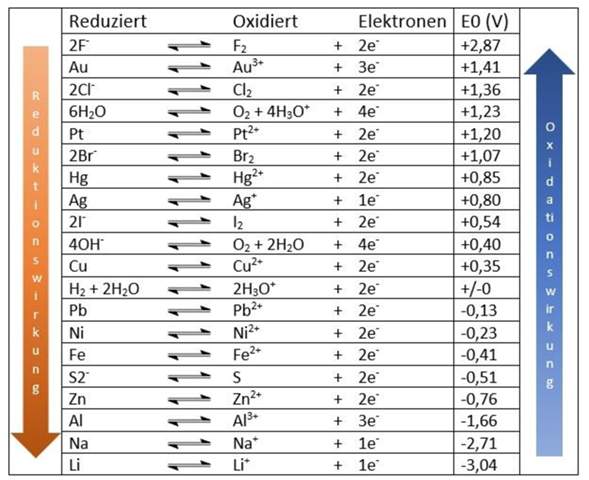
Die Standardpotentiale von Flouridionen zu Flour und von Chloridionen zu Chlor sind doch höher als von Wasser zu Sauerstoff und H3O+. Warum werden dann die Flouridionen nicht zu Flour, aber die Chloridionen zu Chlor?
2 Antworten

Weil die Spannungsreihe nur die halbe Wahrheit ist. Es gibt noch ein (kinetisches) Phänomen, das sich Überspannung nennt. Und die ist bei Sauerstoff ziemlich hoch. Dadurch rutscht das Potential über das von Chlor. Deswegen entsteht bei der Elektrolyse einer HCl-Lösung auch Chlorgas und kein Sauerstoff.
Das Potential von Fluor ist aber auch mit Überspannung noch darüber. Soll heißen, wenn du eine wässrige Fluorid Lösung elektrolysierst, entsteht Sauerstoff, aber kein Fluor.
Fluor kann und wird technisch aber dennoch elektrolytisch gewonnen. Und zwar über Elektrolyse einer Mischung aus Kaliumfluorid und Fluorwasserstoff. Aus oben genannten Gründen muss die Mischung aber natürlich absolut wasserfrei sein.

Weil elementares Fluor mit fast allem reagiert, was nicht bei Drei auf den Bäumen ist. Es ist das stärkste Oxidationsmittel überhaupt und reagiert selbst mit Wasser gemäß:
F2 + 2 H2O --> H2O2 + 2 HF