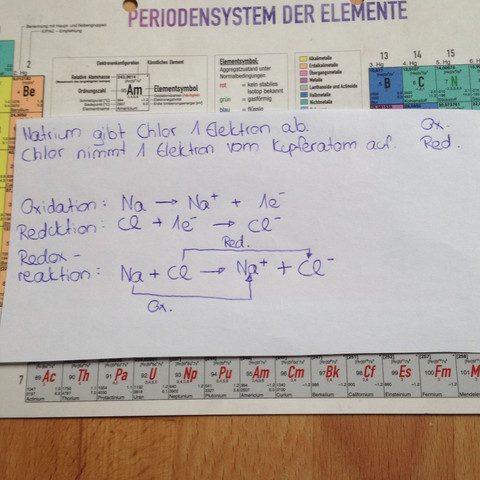
Stimmt die Reaktionsgleichung (Redoxreaktion)?
Stimmt das so? Im Internet stand auch eine Form mit 2Na - wieso?
4 Antworten
Eigentlich ist dies ziemlich richtig, nur dass auf der rechten Seite das Na+ und das Cl- ein zusammenhängenden Stoff, nämlich NaCl, also Natriumchlorid oder besser bekannt als Kochsalz, bildet.
Gruß rofl07
Das stimmt, dass das + und das - entfallen. Schwefel würde in dem Falle, was sehr selten passiert, alle seine 6 Elektronen abgeben, was wirklich kaum passiert, nur bei sehr großen Energieaufwand.
Zink kann glaube ich auch 4 Elektronen abgeben, das ist bei den Nebengruppenelementen sehr unterschiedlich, deshalb lässt sich daraus keine Regel schließen, wie es bei den Hauptgruppe einfach geht. Wenn ein oder sogar beide Stoffe in einer Nebengruppe ist, muss gegeben sein, wie viele Elektronen übergehen, was die Lehrkräfte eigentlich machen.
Ist schon OK. Bloß hast Du Dich verschrieben, Kupfer ist nicht dabei. Wenn man vom elementaren Chlor ausgeht, dann Cl2 und auch entsrechend 2 e- und mit 2 Na
Stimmt so nur des plus auf der rechten Seite muss weg, denn NaCl ist ein zusammenhängender Stoff (Kochsalz), welcher aus den 2 Ausgangsstoffen entstanden ist...
Ach so, dann kommt auch kein + hinters Na oder - hinters Chlor, weil die beiden zusammen ja wieder neutral sind, oder? Wie sieht denn eine Reaktionsgleichung zwischen Schwefel und Chlor aus? Zink ist ja in einer Nebengruppe. Warum gibt Zink dann 2 Elektronen ab? Wie geht das, wenn einer der beiden oder beide Stoffe in einer Nebengruppe ist?
Mann muss das glaub nocch austarieren
Ach so, dann kommt auch kein + hinters Na oder - hinters Chlor, weil die beiden zusammen ja wieder neutral sind, oder?
Wie sieht denn eine Reaktionsgleichung zwischen Schwefel und Chlor aus? Zink ist ja in einer Nebengruppe. Warum gibt Zink dann 2 Elektronen ab? Wie geht das, wenn einer der beiden oder beide Stoffe in einer Nebengruppe ist?