Orbitaltheorie?
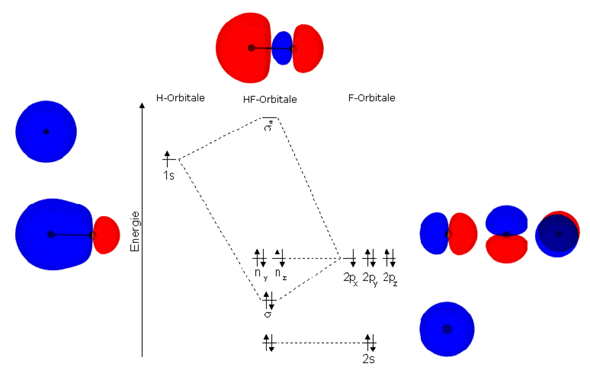
Wieso liegt das 1s-Orbital vom Wasserstoff höher als das von den 2s und 2p-Orbitalen von Fluor?
1 Antwort
Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer
Chemie, Chemie
Der Fluorkern hat 9 Protonen und somit 9 positive Ladungen. Nur 2 davon werden von den Elektronen der ersten Schale abgeschirmt. Daher wirken auf (vorhandene und potentielle) Außenelektronen 7 positive Ladungen. Das ist eine stärkere Anziehung als duch das eine Proton des Wasserstoffs, selbst wenn sie da dichter ran können, in der ersten Schale.
Alle anderen Atom der ersten Hauptgruppe lassen sich ihr Elektron vollständig klauen, nur Wasserstoff will es zumindest teilweise behalten, also teilen. D.H. für Lithium ff. wäre das jeweils äußerste s-Orbital so hoch, dass eine Überlappung wegen der Energiedifferenz unmöglich ist.