Diagramm Chemie beschreiben?
wie kann ich dieses Diagramm beschreiben?
1 Antwort
Moin,
du kannst doch sicher sehen. Und du kannst doch sicher auch schreiben. Und jetzt beschreibst du einfach, was du siehst...
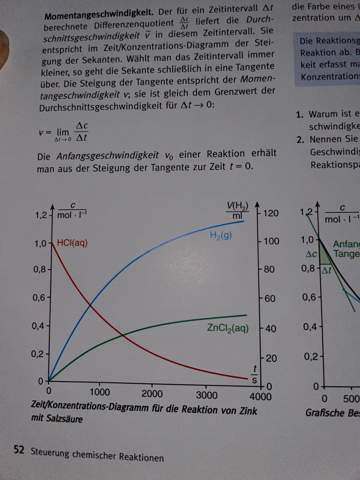
In der Darstellung sieht man ein doppeltes Koordinaten-Diagramm für die Reaktion zwischen Zink und Salzsäure, bei dem einerseits die Stoffmengenkonzentration c [mol • l^–1], andererseits das Volumen V [ml] über der Zeit t [s] aufgetragen ist.
Es sind drei Kurven zu sehen, einmal eine rote für die Konzentration der salzsuren Lösung [HCl (aq)], eine blaue für gasförmigen Wasserstoff [H2 (g)] und eine grüne für in Wasser gelöstes Zinkchlorid [ZnCl2 (aq)].
Während die rote Kurve bei einer Anfangskonzentration von 1 mol/l startet und dann stetig asymptotisch gegen 0 mol/l fällt, beginnen die blaue und die grüne Kurve bei 0 mol/l bzw. 0 ml und steigen dann beide ebenfalls asymptotisch. Dabei steigt die blaue Kurve des Wasserstoffgases stärker (sie läuft gegen 120 ml) als die grüne Kurve des Zinkchlorids, die gegen 0,5 mol/l läuft.
Soweit die Beschreibung des Diagramms. Nun die Interpretation:
Das ist alles logisch, denn am Anfang der Reaktion (Zeitpunkt t = 0 s) ist die salzsaure Lösung noch vollständig konzentriert vorhanden (c = 1 mol/l), während es noch kein Wasserstoffgas (V = 0 ml) und kein Zinkchlorid (c = 0 mol/l) geben kann, da die Reaktion noch gar nicht gestartet ist.
Wenn dann Zink zur Salzsäure gegeben wird, setzt die Reaktion ein. Das Reaktionsschema dazu lautet:
Zn (s) + 2 HCl (aq) ---> ZnCl2 (aq) + H2 (g)↑
Wie man daran sieht, reagiert das Hydrogenchlorid (HCl) mit dem Zink und bildet dabei einerseits Zinkchlorid (ZnCl2) und andererseits Wasserstoff (H2). Das bedeutet, dass die Konzentration an Salzsäure im Verlauf der Reaktionszeit abnimmt (sie wird verbraucht), während zunehmend mehr Zinkchlorid und Wasserstoff gebildet werden (also entstehen). Deshalb fällt die rote Kurve der Salzsäurekonzentration, während die blaue Kurve für den Wasserstoff und die grüne Kurve für das Zinkchlorid beide steigen.
Es ist auch logisch, dass diese Kurven alle asymptotisch verlaufen, denn am Anfang befinden sich viel Salzsäure und viel Zink als Reaktionspartner im Reaktionsraum. Das bedeutet, dass die Wahrscheinlichkeit, dass diese beiden Reaktanten aufeinandertreffen, sehr groß ist. Die Reaktionsgeschwindigkeit ist daher hoch. Die Kurve der Salzsäurekonzentration fällt also schnell. Auch die Kurven für die Wasserstoffgasbildung und die Bildung von Zinkchlorid steigen entsprechend schnell.
Später nimmt aber die Konzentration der Säure ab. Auch die Konzentration an zugefügtem Zink nimmt ab. Es wird also unwahrscheinlicher, dass diese beiden Reaktanten aufeinandertreffen. Daher sinkt die Reaktionsgeschwindigkeit und die Kurve der Salzsäurekonzentration flacht zusehends ab.
Dadurch wird pro Zeitintervall auch nicht mehr so viel Wasserstoff bzw. Zinkchlorid gebildet. Die entsprechenden Kurven werden also auch flacher. Das erklärt den asymptotischen Verlauf der drei Kurven.
Was war daran nun so schwierig? Die Fremdwörter vielleicht? Nun gut, dann lässt du den Fachbegriff „asymptotisch” eben weg und beschreibst das mit „am Anfang fällt die rote Kurve schneller und wird dann immer flacher” oder „am Anfang steigt die blaue Kurve sehr steil und wird dann immer flacher”. Alles andere (bis auf das Reaktionsschema vielleicht) geht doch aus der Abbildung klar hervor. Wie gesagt, du brauchst doch nur zu beschreiben, was du siehst...
LG von der Waterkant
Vielen Dank für deine Mühe, wird mir auch für andere Diagramme hilfreich sein.