Zellspannung eines galv. Elementes - wie geht das?
Kann mir jemand zeigen, wie man die Zellspannung von den beiden galvanischen Elementen bei Standartbedingungen ermitteln kann??
Zn/ZnSO4 // Pb(NO3)2/ Pb
Pt/2Br-,Br2// 2I-,I2/Pt
Also wenn es einzelne Stoffe sind, habe ich es verstanden, aber wenn jetzt hier verschiedene und dann auch noch in Klammern und mit Komma stehen, blicke ich nicht durch :D
Danke für eure Hilfe :)
2 Antworten
Die linke Halbzelle besteht aus einer Zink-Elektrode in Zinksulfat-Lösung (die wiederum Zink- und Sulfat-Ionen enthält, während die rechte Halbzelle aus einer Blei-Elektrode in Bleinitrat-Lösung besteht (die Klammern mit Index 2 geben dabei nur an, dass auf ein Blei(II)-Ion zwei Nitrat-Ionen (NO3-) kommen).
Eine Redox-Reihe mit Redox-Potentialen (Tabelle mit Teilgleichungen und Spannungswerten - ich nehme an, du hast zur Lösung solcher Aufgaben eine zur Hand) hilft dabei herauszufinden, welche Bestandteile der Halbzellen tatsächlich an den Redox-Reaktionen beteiligt sind (und welche nicht!). Damit lassen sich die Angaben dann auf "einzelne Stoffe" reduzieren.
Die untere linke Halbzelle besteht aus einer Platinelektrode und enthält Bromid-Ionen sowie elementarem Brom, während die rechte Halbzelle ebenfalls aus einer Platin-Elektrode besteht und sowohl Iodid-Ionen als auch elementares Iod enthält. Auch hier lassen sich die Angaben auf "einzelne Stoffe" reduzieren (Tipp: Was unterscheidet Platin massgeblich von Zink und Blei?).
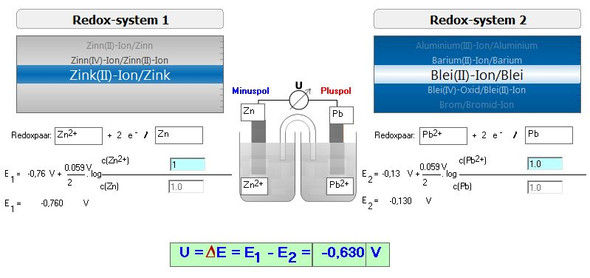
Ich habe Dir in der Anlage eine Versuchsanordnung zu den beiden gewünschten Redoxpaaren simuliert.